
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )

A. 原混合溶液中的CO2-3与AlO-2的物质的量之比为1:2
B. V1:V2=1:5
C. M点时生成的CO2为0.05mol
D. a曲线表示的离子方程式为:AlO-2+H++H2O=Al(OH)3↓
【答案】D
【解析】试题分析:Na2CO3、NaAlO2的混合溶液中逐滴加入1molL-1的盐酸,首先发生反应AlO2-+H++H2O=Al(OH)3↓,a线表示AlO2-,由图可知AlO2-反应完毕,加入盐酸50mL,根据方程式可知n(AlO2-)=n(H+)=0.05L×1mol/L=0.05mol。第二阶段,AlO2-反应完毕,发生反应CO32-+H+=HCO3-,b线表示CO32-,c线表示HCO3-,由图可知CO32-反应完毕,该阶段加入盐酸100mL-50mL=50mL,根据方程式可知n(CO32-)=n(H+)=0.05L×1mol/L=0.05mol。第三阶段,CO32-反应完毕,发生反应HCO3-+H+=CO2↑+H2O,d线表示HCO3-,由图可知HCO3-反应完毕,该阶段加入盐酸150mL-100mL=50mL,根据方程式可知n(HCO3-)=n(H+)。第四阶段,发生反应Al(OH)3+3H+=Al3++3H2O,e线表示Al3+,由图可知Al(OH)3反应完毕,根据方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,该阶段加入盐酸体积为![]() =0.15L=150mL。A、由上述分析可知,原混合溶液中的CO32-与AlO-2的物质的量之比为0.05mol:0.05mol=1:1,A错误;B、原溶液中n(CO32-)=0.05mol,V1时溶液中碳酸氢根离子等于碳酸根离子为0.025ml,由反应CO32-+H+=HCO3-可知,需要盐酸为0.025mol,盐酸的体积为
=0.15L=150mL。A、由上述分析可知,原混合溶液中的CO32-与AlO-2的物质的量之比为0.05mol:0.05mol=1:1,A错误;B、原溶液中n(CO32-)=0.05mol,V1时溶液中碳酸氢根离子等于碳酸根离子为0.025ml,由反应CO32-+H+=HCO3-可知,需要盐酸为0.025mol,盐酸的体积为![]() =0.025L=25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,B错误;C、由上述分析可知M点时溶液中CO32-完全转化为HCO3-,没有CO2生成,C错误;D、由上述分析可知,a曲线表示的离子方程式为:AlO-2+H++H2O=Al(OH)3↓,D正确;答案选D。
=0.025L=25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,B错误;C、由上述分析可知M点时溶液中CO32-完全转化为HCO3-,没有CO2生成,C错误;D、由上述分析可知,a曲线表示的离子方程式为:AlO-2+H++H2O=Al(OH)3↓,D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】在“HI(s)→HI(g)→H2和I2”的变化过程中,被破坏的作用力依次是( )
A. 范德华力、范德华力 B. 范德华力、共价键
C. 共价键、离子键 D. 共价键、共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
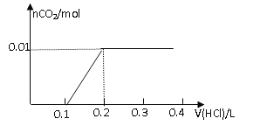
【题目】将0.8g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
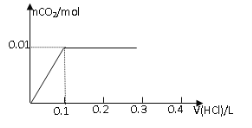
A B
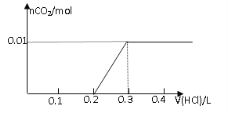
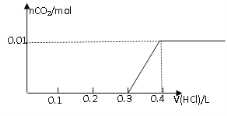
C D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是
A. 使用冰箱保存食物,是利用了化学反应速率理论
B. 化学平衡理论是研究怎样使用有限原料多出产品
C. 使用催化剂,可加快反应速率,目的是提高生产效率
D. 化学反应速率理论是研究怎样提高原料转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关NaClO和NaCl混合溶液的叙述正确的是( )
A. 该溶液中,H+、NH![]() 、SO
、SO![]() 、Br-可以大量共存
、Br-可以大量共存
B. 该溶液中,Ag+、K+、NO![]() 、CH3CHO可以大量共存
、CH3CHO可以大量共存
C. 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+===Cl-+2Fe3++H2O
D. 向该溶液中加入浓盐酸,每产生1 mol Cl2,转移电子约为6.02×1023个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道:氦-3在月球的储量能供地球一万年的能源使用。下列关于32He的说法正确的是
A. 32He原子核内含有3个中子 B. 32He和3 1H互为同位素
C. 32He原子核外有3个电子 D. 32He和42He是两种不同的核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X可能含有Na+、Fe3+、Ca2+、SO42-、 CO32- 、Cl-、I-中的几种离子。为确定其组成,设计并完成以下实验:

根据上述实验,以下推测合理的是
A. 溶液X中是否存在Na+还需要通过焰色反应进一步确认
B. 溶液X中一定不含Fe3+、Ca2+、SO42-
C. 为确定溶液X中是否含有Cl-,可取溶液2加入CCl4充分萃取后,再取上层液体加入AgNO3溶液
D. 溶液X的溶质为Na2CO3和NaI
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com