
分析 (1)化合反应指的是由两种或两种以上的物质反应生成一种新物质的反应,其中部分反应为氧化还原反应,部分为非氧化还原反应;
分解反应是指一种物质分解成两种或两种以上单质或化合物的反应;
复分解反应是由两种化合物互相交换成分,生成另外两种化合物的反应;
氧化还原反应是化学反应前后,元素的化合价有变化的一类反应.
(2)CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2反应中Cu元素的化合价降低,C元素的化合价升高,结合氧化还原反应的概念分析.
解答 解:(1)①Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O该反应属于分解反应;
②2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑该反应属于置换反应;
④CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO该反应属于化合反应;
故答案为:分解反应;置换反应;化合反应;
(2)CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2反应中Cu元素的化合价降低,CuO被还原,生成的Cu为还原产物,C元素的化合价升高,被氧化,则CO发生氧化反应;
故答案为:CO;Cu.
点评 本题考查氧化还原反应及四种基本反应类型,把握反应分类及分类依据为解答的关键,注意氧化还原反应中应该从化合价的角度来分析,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 2molSO2和1molO2在一定条件下充分反应后,混合物的分子数为2NA | |
| B. | 25℃时,1L,pH=1的稀硫酸溶液中含有的H+数目为0.1NA | |
| C. | 用惰性电极电解1L浓度均为0.2mol/L的Cu(NO3)2和AgNO3的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4g金属 | |
| D. | 电解精炼铜(粗铜含铁、锌、银、金杂质),阴极析出1 mol Cu,阳极失去的电子数小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液 | |
| B. | 过量的铁投入到一定量的稀硝酸中,充分反应后取上层清液于试管中,滴加KSCN溶液,溶液显红色 | |
| C. | 制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁 | |
| D. | 向CuSO4溶液中滴入过量NaOH溶液充分反应后,将混合液体倒入蒸发皿中加热煮沸一会,然后冷却、过滤,滤纸上的物质为“蓝色固体” |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向某溶液中加入BaCl2溶液,有白色沉淀,则原溶液一定存在Ag+或SO42- | |
| B. | 根据纤维在火焰上燃烧产生的气味,可确定该纤维是否为蛋白质纤维 | |
| C. | 两份常温下均为饱和溶液(一份是NaOH溶液,一份是氢氧化钾溶液),上述两份饱和溶液可通过加入少量的NaOH固体而鉴别出 | |
| D. | 某矿石中加入足量的盐酸,根据放出的二氧化碳气体,可证明该矿石一定含有碳酸钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 萃取操作时,选择的萃取剂的密度必须比水大 | |
| D. | 分液操作时,上层液体从分液漏斗下口放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加KSCN显红色的溶液中:K+、NH4+、Cl-、S2- | |
| B. | pH=1的溶液中:K+、Fe3+、Cl-、NO3- | |
| C. | “84”消毒液的溶液中:Fe2+、Cl-、Ca2+、Na+ | |
| D. | 含有大量NH4+的溶液中:Ba2+、K+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和NO2都是有用的化工原料,因此目前都是将汽车尾气中的氮氧化合物收集后制备硝酸以防止污染空气 | |
| B. | 由于HClO具有漂白性,因此工业上常用Cl2的水溶液来漂白纸浆、毛、丝、草帽辫 | |
| C. | 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,消毒原理相同,都利用了强氧化性 | |
| D. | 金属钠通常被保存在煤油中,以隔绝空气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
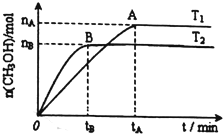 科学家利用太阳能分解水生产的氢气在催化剂作用下与二氧化碳反应生成甲醇(CH3OH).已知H2(g)、CO(g)和CH3OH(l)的燃烧热分别为285.8kJ•mol-1、283.0kJ•mol-1和726.5kJ•mol-1.
科学家利用太阳能分解水生产的氢气在催化剂作用下与二氧化碳反应生成甲醇(CH3OH).已知H2(g)、CO(g)和CH3OH(l)的燃烧热分别为285.8kJ•mol-1、283.0kJ•mol-1和726.5kJ•mol-1.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com