
分析 (1)NH3与灼热的CuO反应,生成N2,Cu和化合物A,根据元素守恒知,A为H2O;
(2)该反应中N元素化合价由-3价变为0价、Cu元素化合价由+2价变为0价,转移电子数是6,所以该反应方程式为2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3H2O+3Cu;
(3)该反应中氨气失电子作还原剂,CuO得电子作氧化剂,n(NH3)=$\frac{17g}{17g/mol}$=1mol,根据氨气和CuO之间的关系式计算消耗CuO的质量.
解答 解:(1)NH3与灼热的CuO反应,生成N2,Cu和化合物A,根据元素守恒知,A为H2O,答:A为H2O;
(2)该反应中N元素化合价由-3价变为0价、Cu元素化合价由+2价变为0价,转移电子数是6,所以该反应方程式为2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3H2O+3Cu,其转移电子方向和数目为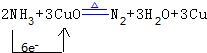 ,
,
答:其转移电子方向和数目为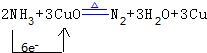 ;
;
(3)该反应中氨气失电子作还原剂,CuO得电子作氧化剂,n(NH3)=$\frac{17g}{17g/mol}$=1mol,根据氨气和CuO之间的关系式得消耗m(CuO)=$\frac{1mol}{2}×3×80g/mol$=120g,
答:消耗CuO的质量是120g.
点评 本题考查氧化还原反应有关计算,侧重考查学生分析计算能力,明确各个物理量之间的关系是解本题关键,难点是(2)题电子转移方向和数目的标注.


科目:高中化学 来源: 题型:选择题

| A. | 图1中醋酸电离平衡常数:a点的比b点的小 | |
| B. | 图1中醋酸溶液的pH:a点的比b点的小 | |
| C. | 图2中c点对应的溶液为Fe(OH)3的不饱和溶液 | |
| D. | 由图2可知,欲除去CuSO4溶液中的Fe3+,可向溶液中加入CuO,调节pH约为4左右 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度 | B. | 恒容时,再通入2amolC和2amolD | ||
| C. | 恒压时,再通入2amolC和2amolD | D. | 恒容时,再通入amolA和amolB |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5:4 | B. | 4:5 | C. | 5:12 | D. | 12:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
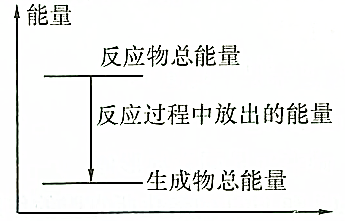
| A. | 反应过程中的能量关系可用如图表示 | |
| B. | 1mol锌所含的能量高于1mol H2 所含的能量 | |
| C. | 若将其设计为原电池,则锌为正极 | |
| D. | 若将其设计为原电池,当有32.5g锌溶解时,正极放出气体一定为11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙烯制溴乙烷:CH2CH2+Br2→CH2BrCH2Br | |
| B. | 乙醇催化氧化:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3COH+2H2O | |
| C. | 苯与氢气加成: +3H2$\stackrel{Ni}{→}$ +3H2$\stackrel{Ni}{→}$ (环己烷) (环己烷) | |
| D. | 从海带中提取碘:H2O2+2I-+2H+=I2+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com