
���������������
�����ȶ��ԣ�H2O��HF��H2S ��Fe�Ǹ���Ԫ�� ��IIA��Ԫ�ص���������������ϡ������Ԫ�ص�ԭ�Ӿ�����ͬ�ĺ�������Ų� ��Ԫ�����ڱ��д�IIIB��IIB��10�����е�Ԫ�ض��ǽ���Ԫ�� �ݶ����ԭ���У�����˽Ͻ����������˶��ĵ��������ϸ� ����֪H2SO4(aq)��2NaOH(aq)��2H2O(l)��Na2SO4(aq)��H����114.6kJ/mol�����к���Ϊ-57.3kJ��mol-1 �������ǽ���Ԫ��ԭ�Ӽ�ֻ�����γɹ��ۼ�����������Ԫ�صĻ�������һ����������
A���ڢܢ� B���٢ݢ� C���ڢۢ� D���٢ڢݢ�
D
��������
����������ٷǽ�������F��O��S�������ȶ��ԣ�HF��H2O��H2S������Fe�ǵڢ���Ԫ�أ�����IIA��Ԫ�ص���������������ϡ������Ԫ�ص�ԭ�Ӿ�����ͬ�ĺ�������Ų�����ȷ����Ԫ�����ڱ��д�IIIB��IIB��10�����е�Ԫ�ض��ǽ���Ԫ�أ���ȷ���ݶ����ԭ���У�����˽Ͻ����������˶��ĵ��������ϵͣ������к�������һ�������£�ϡ��Һ�У�ǿ���ǿ�Ӧ����1molˮʱ���ų�����������֪H2SO4(aq)��2NaOH(aq)��2H2O(l)��Na2SO4(aq)��H����114.6kJ/mol�����к���Ϊ57.3kJ��mol-1����ȷ���������ǽ���Ԫ��ԭ�Ӽ�ֻ�����γɹ��ۼ�����������Ԫ�صĻ������в�һ�����������������Ȼ����к������Ӽ�������ѡD��
���㣺����Ԫ�������ɡ���ѧ�����к����Լ�Ԫ�����ڱ��Ľṹ


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
��ӦA(g)+3B(g)  2C(g)+2D(g)���ڲ�ͬ����²�÷�Ӧ���ʣ����з�Ӧ����������
2C(g)+2D(g)���ڲ�ͬ����²�÷�Ӧ���ʣ����з�Ӧ����������
A����(D)=0.4 mol / ?L��s? B����(C)=0.5 mol / ?L��s?
C����(B)=0.6 mol / ?L��s? D����(A)=0.15 mol / ?L��s?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ֣���и�����һ������Ԥ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���н���ʵ����ʵ�Ļ�ѧ����ʽ�����ӷ���ʽ����ȷ����
A��������������ˮ��ɱ��������Cl2+H2O HCl+HClO
HCl+HClO
B������NO2��������ˮ�У���ɫ���2NO2(g)  N2O4(g)
N2O4(g)  H��0
H��0
C����Ba(OH)2��Һ�еμ�NaHSO4��Һ������Һ�����ԣ�OH-+ Ba2++ H++SO42- = BaSO4��+ H2O
D��ͭƬ�ܽ���KNO3��ϡ����Ļ��Һ�У�3Cu + 8H+ + 2NO3- === 3Cu2+ + 2NO�� + 4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��У���˸�����һ���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ���ں����ø�ѹ������ػ����Ϸ�չ������һ�ֽ����⻯������� (MH��Ni���Ե��)�������й�˵������ȷ����

A���ŵ�ʱ������ӦΪ��NiOOH��H2O��e��=Ni(OH)2��OH��
B���ŵ�ʱ������ӦΪ��MH��OH�D-2e��=H2O��M+
C�����ʱ��������������������Ҫ����缫��Ӧ
D�����ʱ��ص���������ֱ����Դ���������õ����ӷ�����ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ������
��10�֣������꿪���ļ״�ȼ�ϵ���Dz��ò����缫����������е����ӽ���Ĥֻ�������Ӻ�ˮ����ͨ�����乤��ԭ����ʾ��ͼ���£�
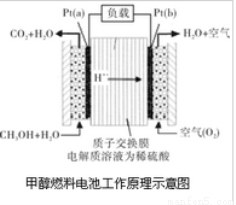
��ش��������⣺
��1��Pt��a���缫��Ӧ�����ĵ缫��ӦΪ ��Pt��b���缫���� ��Ӧ�����������ԭ�������缫��ӦΪ ��
��2����ص��ܷ�Ӧ����ʽΪ ��
��3������õ�ع���ʱ��·��ͨ��2mol���ӣ������ĵ�CH3OH�� mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�±��и�������֮��ͨ��һ����Ӧ������ʵ����ͼ��ʾת����ϵ����


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ٵĻ�����PdCl2ͨ����ѧ��Ӧ������������ж�����CO���÷�Ӧ�ķ�Ӧ�����������У�CO��Pd,H2O��HCl��PdCl2��һ��δ֪��X������˵��������
A���÷�Ӧ�����»�ԭ�ԣ�CO��Pd B��δ֪����XΪCO2
C��ÿת��1mole-ʱ������2molX D����Ӧ��CO����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�����ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
H2S2O3��һ�����ᣬʵ��������0.01 mol��L��1��Na2S2O3��Һ�ζ�I2��Һ�������ķ�ӦΪI2+2Na2S2O3 =2NaI+Na2S4O6������˵����������

A���õζ����ü�����ָʾ��
B��Na2S2O3�Ǹ÷�Ӧ�Ļ�ԭ��
C���õζ���ѡ����ͼ��ʾװ��
D���÷�Ӧ��ÿ����2mol Na2S2O3������ת����Ϊ4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015������ʡ��һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
һЩװ�л�ѧ���ʵ������ϳ�����Σ�ջ�ѧƷ�ı�־�����б�־�У�Ӧ����װ�оƾ��������ϵ���
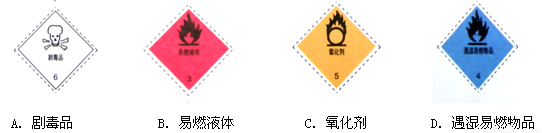
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com