
对已经达到化学平衡的反应:COCl2(g) 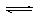 CO(g) + Cl2(g),△H>0 当反应达到平衡时下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减小压强 ⑤加催化剂,其中能提高COCl2(g)转化率的是 ( )
CO(g) + Cl2(g),△H>0 当反应达到平衡时下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减小压强 ⑤加催化剂,其中能提高COCl2(g)转化率的是 ( )
A.①⑤ B.①④ C.②③ D.③⑤
 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
下图表示某气态单质A及其化合物之间的转化关系 (某些产物和反应条件已略去)。
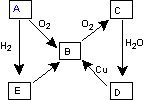 (1)A单质的电子式
(1)A单质的电子式
(2)写出E生成B的化学方程式:
。
(3)①写出由D生成B的离子方程式 。
②常温下D和E恰好完全反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某KCl、MgCl2、Mg(NO3)2形成的混合中, c(K+)=0.20mol/L, c(Mg2+)=0.25mol/L,
c(Cl-)=0.20mol/L, 则c(NO3-)为
A. 0.15mol/L B. 0.10mol/L C. 0.25mol/L D. 0.50mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
现有NaOH和Na2CO3固体混合物18.6g ,加入足量2mol/L 的盐酸,放出标准状况下的气体2.24L,则原固体混合物中NaOH和Na2CO3的物质的量各为多少?反应后溶液加水至500mL,则溶液中Na+的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释至所需浓度,如此操作的目的是 ( )
A.防止硫酸铁分解 B.抑制硫酸铁水解 C.提高硫酸铁的溶解度 D.提高溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实能说明乙酸(CH3COOH) 属于弱酸的是 ( )
① 1mol/L CH3COOH的 pH=2 ②乙酸能与水以任意比互溶
③ 20mL 1mol/L CH3COOH 与20mL 1mol/LNaOH恰好中和
④ CH3COONa溶液的pH>7
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
)(1)常温下,将0.2 mol/L HCl溶液与0.2 mol/L氨水等体积混合(忽略混合后溶液体积的变化),测得混合后溶液的pH=6,试回答以下问题:
(1)混合后溶液呈酸性的原因是(用离子方程式回答) 。
(2)混合后溶液中由水电离出的c(OH-)为
(3)常温下,将0.2 mol·L-1的盐酸与 0.2mol·L-1的氨水混合,若所得的混合溶液中的pH=7,下列关系正确的是
A、[Cl-]>[NH4+]> [H+] > [OH-] B、[NH4+]>[Cl-]>[OH-]>[H+]
C、[Cl-]=[NH4+]>[H+]=[OH-] D、[NH4+]>[Cl-]>[H+]>[OH-]
(4)由电离常数可知酸性强弱: CH3COOH>H2CO3>HCO3-,则浓度相同的下列溶液碱性由强到弱顺序为: (填序号)
①CH3COONa ② NaHCO3 ③ Na2CO3
(5)将氯化铁溶液蒸干、灼烧,最后得到的固体是 。
(6)Cu(OH)2(s) 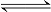 Cu2+(aq)+2OH-(aq),在常温下Ksp( Cu(OH)2)=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol•L-1的CuSO4溶液中加入NaOH溶液,调整pH最小到 。
Cu2+(aq)+2OH-(aq),在常温下Ksp( Cu(OH)2)=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol•L-1的CuSO4溶液中加入NaOH溶液,调整pH最小到 。
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是
A.生成42.0LN2(标准状况)
B.有0.250molKNO3被氧化
C.转移电子的物质的量为1.25mol
D.被氧化的N原子的物质的量为3.75mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com