
【题目】石油产品中除含有H2S外,还含有各种形态的有机硫,如COS、CH3SH。回答下列问题:
(1)CH3SH(甲硫醇)的电子式为________。
(2)一种脱硫工艺为:真空K2CO3—克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3,该反应的平衡常数的对数值为lgK=_____(已知:H2CO3 lgK1=-6.4,lgK2=-10.3;H2SlgK1=-7,lgK2=-19)。
②已知下列热化学方程式:
a.2H2S(g)+3O2(g)=2SO2(g)+ 2H2O(l) △H1=-1172kJ/mol
b.2H2S(g)+O2(g)=2S(s)+2H2O(l) △H2=-632kJ/mol
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为__________。
(3)Dalleska等人研究发现在强酸溶液中可用H2O2氧化COS。该脱除反应的化学方程式为______________。
(4)COS水解反应为COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H=-35.5kJ/mol。
CO2(g)+H2S(g) △H=-35.5kJ/mol。
用活性α-Al2O3催化,在其它条件相同时,改变反应温度,测得COS水解转化率如图1所示;某温度时,在恒容密闭容器中投入0.3molH2O(g)和0.1molCOS,COS的平衡转化率如图2所示。
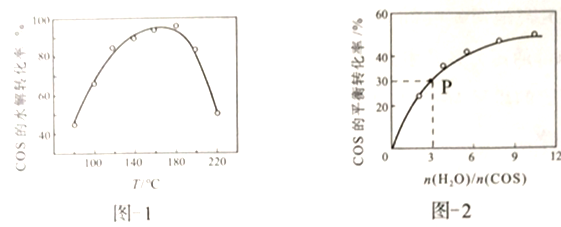
①图1活性α-Al2O3催化水解,随温度升高转化率先增大后又减小的可能原因是________。
②由图2可知,P点时平衡常数为K=______(填数字)。
③活性α-Al2O3催化水解,为提高COS的转化率可采取的措施是____________。
【答案】 ![]() 3.3 2H2S(g) + SO2(g) = 3S(s) +2H2O(l) △H=-362 kJ·mol-1 COS+4H2O2 =CO2+H2SO4+3H2O 开始温度低,催化剂活性小,到160℃活化剂活性最大,继续升温,催化剂活性降低且平衡向逆反应方向移动 0.0476 控制温度约160℃并增大n(H2O)/n(COS)
3.3 2H2S(g) + SO2(g) = 3S(s) +2H2O(l) △H=-362 kJ·mol-1 COS+4H2O2 =CO2+H2SO4+3H2O 开始温度低,催化剂活性小,到160℃活化剂活性最大,继续升温,催化剂活性降低且平衡向逆反应方向移动 0.0476 控制温度约160℃并增大n(H2O)/n(COS)
【解析】(1)CH3SH(甲硫醇)属于共价化合物,其电子式为![]() 。
。
(2)一种脱硫工艺为:真空K2CO3—克劳斯法。
① K2CO3+H2S=KHS+KHCO3
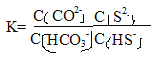 =
=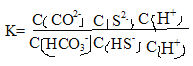 =
=![]() =10-7/10-10.3=103.3 lgK=3.3。答案:3.3。
=10-7/10-10.3=103.3 lgK=3.3。答案:3.3。
②已知下列热化学方程式:
根据a.2H2S(g)+3O2(g)=2SO2(g)+ 2H2O(l) △H1=-1172kJ/mol
b.2H2S(g)+O2(g)=2S(s)+2H2O(l) △H2=-632kJ/mol
![]() =-632 kJ/mol
=-632 kJ/mol![]() 3-(-1172kJ/mol)/2=-362 kJ·mol-1
3-(-1172kJ/mol)/2=-362 kJ·mol-1
故2H2S(g) + SO2(g) = 3S(s) +2H2O(l) △H=-362 kJ·mol-1
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为2H2S(g) + SO2(g) = 3S(s) +2H2O(l) △H=-362 kJ·mol-1。
(3)Dalleska等人研究发现在强酸溶液中可用H2O2氧化COS。该脱除反应的化学方程式为COS+4H2O2 =CO2+H2SO4+3H2O
(4)①图1活性α-Al2O3催化水解,催化剂与温度有一个临界点,高于这个临界点,催化剂的活性降低。由图可知开始温度低,催化剂活性小,到160℃活化剂活性最大,继续升温,催化剂活性降低且平衡向逆反应方向移动。
② COS(g)+H2O(g)![]() CO2(g)+H2S(g
CO2(g)+H2S(g
初始量 0.1 0.3 0 0
变化量 X X X X
平衡量 0.1-X 0.3-X X X
P点时COS转化率为30![]() ,所以X=0.03mol平衡常数为K=0.3
,所以X=0.03mol平衡常数为K=0.3![]() 0.3/0.07
0.3/0.07![]() 0.27=0.0476
0.27=0.0476
③COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H=-35.5kJ/mol。为提高可使化学平衡向正反应方向移动,根据影响化学平衡移动的因素温度,压强 浓度,由方程式可知压强不能改变平衡移动,所以可以增加水蒸气的浓度,温度升高COS的转化率降低,所以控制温度约160℃并增大n(H2O)/n(COS)即可。
CO2(g)+H2S(g) △H=-35.5kJ/mol。为提高可使化学平衡向正反应方向移动,根据影响化学平衡移动的因素温度,压强 浓度,由方程式可知压强不能改变平衡移动,所以可以增加水蒸气的浓度,温度升高COS的转化率降低,所以控制温度约160℃并增大n(H2O)/n(COS)即可。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)在3种有机物 ① ![]() 、② CH2=CH2、③葡萄糖中,从石油中提取的重要有机溶剂是______(填序号,下同),可用作生产塑料袋的是_______。为人体提供能量的物质是_______。
、② CH2=CH2、③葡萄糖中,从石油中提取的重要有机溶剂是______(填序号,下同),可用作生产塑料袋的是_______。为人体提供能量的物质是_______。
(2)在3种无机物 ① Na2SiO3、②HNO3、③ SO2中,可用作阻燃的是______(填序号,下同),可用于漂白织物的是______, 可用作生产炸药的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。

Ⅰ.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)碳酸钙悬浊液中分离出碳酸钙___________;
(2)氯化钠溶液中分离出氯化钠___________;
(3)分离植物油和水___________;
(4)海水淡化___________;
(5)氯化钠溶液中分离出水___________;
(6)除去自来水中的Cl﹣等杂质___________;
(7)从碘水中分离出I2___________。
Ⅱ.碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的是___________。
A.酒精 B.苯
②分液漏斗在使用前必须先___________。
③查资料得知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的______端口放出,有机层应由分液漏斗的______端口放出(此问填“上”或者“下”)
(2)蒸馏
①装置A中a的名称是_______,冷凝装置中冷凝水应该________口进(填“上”或“下”),这样做的目的是________________________,装置C在分液时为使液体顺利滴下,除打开漏斗下端的旋塞外,还应进行的具体操作是__________________________。
②已知碘和四氯化碳的熔沸点数据如下表
熔点 | 沸点 | |
碘 | 113.7℃ | 184.3℃ |
四氯化碳 | -22.6℃ | 76.8℃ |
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是___________。
Ⅲ. 海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

问题一:粗盐中含Ca2+、Mg2+、SO42﹣等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发正确的操作顺序是__________(填选项字母).
⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
问题二:由海水到氯化钠晶体的实验过程中要用到的主要装置是_________________(从给定的四种装置中选择,填字母)。
问题三:粗盐中含有少量泥沙、CaCl2、MgCl2及硫酸盐,将粗盐溶解后,先过滤将泥沙除去,再检验滤液中的SO42﹣,检验滤液中的SO42﹣的实验操作和现象是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯可提高花或果的芳香气味,故常用于化妆品工业和食品工业。乙酸苯甲酯可以用下面的设计方案合成:
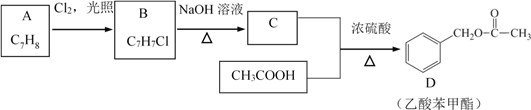
请回答:
(1)乙酸苯甲酯中官能团的名称是________。
(2)A到B的反应类型是________。
(3)由C生成D的反应方程式为________。
(4)满足下列条件的D的同分异构体为________。(写出一种即可)
① 与FeCl3溶液反应显紫色
② 1mol D可以与4mol H2发生加成反应
③ D的核磁共振氢谱有四组峰,峰面积比为6:2:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol/L的一元碱BOH与等浓度的HCl溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
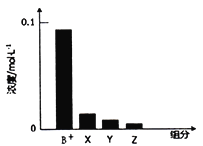
A. BOH为强碱 B. 该混合液pH=7
C. 图中X表示BOH,Y表示H+,Z表示OH- D. 该混合溶液中:c(Cl-)=c(Y)+c(B+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,现有![]() ;
;![]() 个HCl分子;
个HCl分子;![]() ;
;![]()
![]() ,对这四种气体的关系有以下四种表述:其中正确的是 ______ .
,对这四种气体的关系有以下四种表述:其中正确的是 ______ .
a.体积:![]()
b.物质的量:![]()
c.质量:![]()
d.氢原子个数:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数的值用NA表示,则:
(1)该气体的物质的量为________。
(2)该气体所含原子总数为________。
(3)该气体在标准状况下的体积为________。
(4)该气体在标准状况下的密度为________。
(5)该气体一个分子的质量为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com