
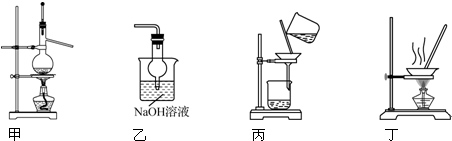
| A. | 用装置甲以乙醇和浓硫酸为原料制乙烯 | |
| B. | 用装置乙吸收某些实验尾气中的二氧化硫 | |
| C. | 用装置丙分离Cl2与KI溶液反应生成的碘 | |
| D. | 用装置丁蒸干NH4Cl饱和溶液获取NH4Cl晶体 |
分析 A.以乙醇和浓硫酸为原料制乙烯,温度计用于测量液体的温度;
B.二氧化硫易溶于氢氧化钠溶液,应防止倒吸;
C.碘易溶于有机溶剂,应用萃取的方法分离;
D.注意氯化铵易分解.
解答 解:A.以乙醇和浓硫酸为原料制乙烯,需加热到170℃,温度计用于测量液体的温度,故A错误;
B.二氧化硫易溶于氢氧化钠溶液,应防止倒吸,可完成实验,故B正确;
C.碘易溶于有机溶剂,应用萃取的方法分离,而过滤用于分离固体和液体,故C错误;
D.氯化铵加热易分解,直接蒸干不能得到氯化铵,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的制备、混合物分离提纯等,把握物质的性质、反应原理、实验基本技能为解答的关键,侧重实验评价分析的考查,注意实验装置的作用,题目难度不大.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源: 题型:解答题
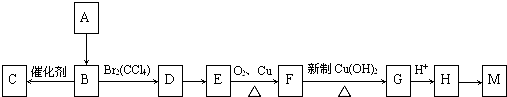
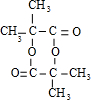 .
.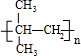 ;E→F:2(CH3)2C(OH)-CH2OH+O2$→_{△}^{Cu}$2(CH3)2C(OH)-CHO+2H2O.
;E→F:2(CH3)2C(OH)-CH2OH+O2$→_{△}^{Cu}$2(CH3)2C(OH)-CHO+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于有气体参与的化学平衡体系,增大压强,反应速率一定加快 | |
| B. | 常温下,反应4Fe(OH)2(S)+2H2O(l)+O2(g)=4Fe(OH)3(S)的△H<0,△S<0 | |
| C. | 用0.1mol/L醋酸滴定0.lmol/L NaOH溶液至中性时:c(CH3COO -)+c(CH3COOH)<c(Na+) | |
| D. | 向纯水中加入盐类物质,有可能促进水的电离平衡,但不可能抑制水的电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位物质的量的气体所占的体积就是气体摩尔体积 | |
| B. | 摩尔是物质的量的单位 | |
| C. | 阿伏加德罗常数就是6.02×1023 | |
| D. | CO2的摩尔质量为44g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
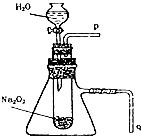 用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ).
).
 .
. .
. .
. 、
、 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 为了探索外界条件对反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1的影响,若保持气体总质量不变,在温度为T1、T2时,通过实验得到平衡体系中NO2的体积分数随压强变化曲线,实验结果如图所示.下列说法正确的是( )
为了探索外界条件对反应2NO2(g)?N2O4(g)△H=-57kJ•mol-1的影响,若保持气体总质量不变,在温度为T1、T2时,通过实验得到平衡体系中NO2的体积分数随压强变化曲线,实验结果如图所示.下列说法正确的是( )| A. | a、c两点气体的平均相对分子质量:a>c | |
| B. | a、c两点气体的颜色:a浅,c深 | |
| C. | b、c两点的平衡常数:Kb=Kc | |
| D. | 状态a通过升高温度可变成状态b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com