
| A.反应中共转移电子1.5 mol | B.反应中共消耗锌65 g |
| C.气体A为SO2和H2的混合物 | D.气体A中SO2和H2的体积比为4∶1 |


科目:高中化学 来源:不详 题型:实验题
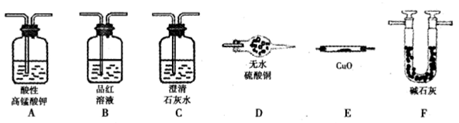
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4CuSO3中硫元素被氧化 | B.刺激性气味的气体是二氧化硫 |
| C.刺激性气味的气体是氨气 | D.该反应中硫酸作氧化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. SO42- SO42- | B.S | C.SO32- | D.S2- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al | B.Zn | C.Fe | D.Mg |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 时间 | 开始 | 8 h后 | 16 h 后 | 24 h后 | 32 h后 | 4O h后 | 48 h后 |
| pH | 5.O | 4.8 | 4.5 | 4.3 | 4.2 | 4.O | 4.O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
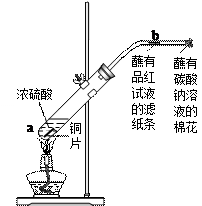
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com