
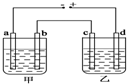
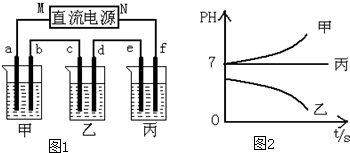
 甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )
甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )| A. | 甲槽中溶液是H2SO4,乙槽中溶液是NaOH | |
| B. | 甲槽中溶液是NaOH,乙槽中溶液是AgNO3 | |
| C. | 甲槽中溶液是AgNO3,乙槽中溶液是CuSO4 | |
| D. | 甲槽中溶液是CuSO4,乙槽中溶液是H2SO4 |
分析 根电源正极相连的是电解池的阳极,所以b、d是电解池的阳极,发生氧化反应,而a、c是电解池的阴极发生还原反应,以此解答该题.
解答 解:A、乙槽中溶液是NaOH,是电解水,所以c极板质量不变,故A错误;
B、甲槽中溶液是NaOH,则甲槽是电解水,a极是氢离子放电生成氢气,乙槽中溶液是AgNO3,则c极是银离子放电生成单质银,故B正确;
C、甲槽中溶液是甲槽中溶液是AgNO3,a极是银离子放电生成金属银,极板质量增加,无气体产生,故C错误;
D、甲槽中溶液是CuSO4,a极是铜离子放电生成单质铜,板质量增加,无气体产生,故D错误;
故选B.
点评 本题考查电化学中的电解池,学生只要掌握电解池的反应原理和电极的判断就可以迅速解题了,比较容易.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ②③④ | C. | ①③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 7:2 | B. | 4:5 | C. | 5:4 | D. | 2:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
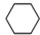 (g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$
(g)$?_{高温}^{Pt-Sn/Al_{2}O_{3}}$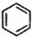 (g)+3H2(g)△H>0,若该反应在恒容的密闭容器中进行,下列有关该反应的图象判断正确的是( )
(g)+3H2(g)△H>0,若该反应在恒容的密闭容器中进行,下列有关该反应的图象判断正确的是( )| A. |  | B. | 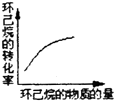 | C. | 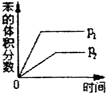 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去MgCl2溶液中的Fe3+,可向溶液中加入氨水调节pH | |
| B. | 除去污水中的金属离子Cu2+、Hg2+,可向溶液中加入FeS | |
| C. | 除去Cl2中混有的HCl,可以将气体通入饱和氯化钠溶液 | |
| D. | 除去CaCO3中的少量CaSO4,可以向其中加入足量饱和Na2CO3溶液后过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol某气体的体积为22.4L,该气体的状况不一定是标准状况 | |
| B. | 1 mol H2O中含有的质子数为9NA | |
| C. | 2.4g镁由原子变为离子时,失电子为0.1NA | |
| D. | 将1mol CO2气体变成固体,其所含的分子数小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有的化学反应都有能量变化 | |
| B. | 只要有能量的变化,一定发生了化学反应 | |
| C. | 据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物YR4中各原子均满足8电子稳定结构 | |
| B. | 对应原子半径:Z<W<R | |
| C. | W与X、W与Y形成的化合物化学键类型完全相同 | |
| D. | Y的最高价氧化物对应的水化物是弱酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com