
【题目】(1)某浓度的氨水中存在下列平衡:NH3H2O![]() NH4++OH-,若想增大NH4+的浓度,而不增加OH-的浓度,应采取的措施是__。(填序号)
NH4++OH-,若想增大NH4+的浓度,而不增加OH-的浓度,应采取的措施是__。(填序号)
①适当升高温度②加入NH4Cl固体③通入NH3④通入少量HCl气体
(2)常温下,有pH相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,产生等量的氢气时,所需要的时间:醋酸_____盐酸(填“>”、“=”或“<”)。
(3)已知电离平衡常数,H2SO3:K1 = 1.54×10-2,K2 = 1.02×10-7;H2CO3:K1 = 4.3×10-7,K2 = 5.6×10-11; CH3COOH:Ka=1.8×105。
① HSO3-的电离平衡常数表达式为:______。
② H2SO3溶液与NaHCO3溶液反应的主要离子方程式为_________。
③在25℃的条件下,向0.1mol·L1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO)=5∶9,此时溶液pH=___。
【答案】②④ < K2=![]() H2SO3 + HCO3- = HSO3- + CO2↑+ H2O 5
H2SO3 + HCO3- = HSO3- + CO2↑+ H2O 5
【解析】
(1)①适当升高温度,平衡正向移动,c(NH4+)增大,c(OH-)增大,故错误;
②加入氯化铵固体,c(NH4+)增大,平衡逆向移动,c(OH-)减小,故正确;
③向氨水中通入氨气,c(NH4+)增大,c(OH-)增大,故错误;
④通入少量HCl气体,HCl电离产生的H+消耗OH-,平衡逆向移动,c(NH4+)增大,c(OH-)减小,故正确;
答案选②④;
(2)常温下,pH相等的醋酸和盐酸,醋酸浓度大于盐酸,所以pH、体积相等的醋酸和盐酸,醋酸的物质的量大于盐酸,则分别与足量的锌反应醋酸放出的氢气多,且醋酸产生氢气的速率更快,产生等量的氢气时,所需要的时间:醋酸<盐酸;
(3)①根据电离方程式HSO3-![]() H+ + SO32-可知,HSO3-的电离平衡常数表达式为:K2=
H+ + SO32-可知,HSO3-的电离平衡常数表达式为:K2=![]() ;
;
②根据H2SO3:K1 = 1.54×10-2,K2 = 1.02×10-7;H2CO3:K1 = 4.3×10-7,K2 = 5.6×10-11;可知酸性:H2SO3> H2CO3> HSO3-,H2SO3溶液与NaHCO3溶液反应的主要离子方程式为H2SO3 + HCO3- = HSO3- + CO2↑+ H2O;
③在25℃的条件下,向0.1mol·L1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO)=5∶9,此时溶液中Ka=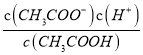 =
=![]() ×
×![]() =1.8×105,故
=1.8×105,故![]() =1.0×105mol/L,pH=5。
=1.0×105mol/L,pH=5。


科目:高中化学 来源: 题型:
【题目】固体A的化学式为NH5,其所有原子的最外电子层结构都符合相应稀有气体元素原子的最外电子层结构,则下列有关说法不正确的是( )
A.1 mol NH5中含有5NA个N—H键(设NA表示阿伏加德罗常数的值)
B.NH5中既有共价键又有离子键
C.NH5的电子式为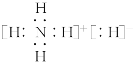
D.NH5与水反应的离子方程式为NH4++H-+H2O=NH3·H2O+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
完成下列填空:
(1)硫原子的核外电子排布式为__,硫原子的核外电子占有__个轨道,Z元素在元素周期表中的位置为__,Y原子核外有______种能量不同的电子。
(2)H2S分子中H-S键键角为92°,说明H2S分子是__(填“极性”“非极性”)分子。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是__。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫单质得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成0.1molX的最高价化合物,恢复至室温,放热68.7kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式___。
(5)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式解释产生该现象的原因:___;在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产生该现象的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g)![]() CO2(g)+N2(g),平衡时c (NO)与温度T的关系如图所示,则下列说法正确的是
CO2(g)+N2(g),平衡时c (NO)与温度T的关系如图所示,则下列说法正确的是
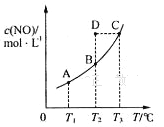
A.该反应的△H>0
B.在T2时,若 反 应 体 系 处于 状 态D ,则 此 时v正>v逆
C.若状态B、C、D的压强分别为PB、PC 、PD ,则PC=PD>PB
D.若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,加水冲稀时c(H+)/c(OH-)的值明显减小的溶液中,一定能大量共存的离子组是
①K+、Cl-、NO![]() 、CH3COO- ②Na+、Fe2+、I-、SO
、CH3COO- ②Na+、Fe2+、I-、SO![]()
③Ba2+、Cl-、NO![]() 、Na+ ④Na+、Ca2+、Cl-、HCO
、Na+ ④Na+、Ca2+、Cl-、HCO![]()
⑤K+、SO![]() 、Cl-、NO
、Cl-、NO![]()
A. ①③⑤ B. ②③ C. ②④ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮族元素包括N、P、As、Sb和Bi五种元素。
(1)下列关于氮族元素的说法正确的是___。
a.N2可用于填充霓虹灯。其发光原理是电子从能量较低的轨道跃迁到能量较高的轨道,以光的形式释放能量
b.P、Na、S三种元素的第一电离能由大到小的顺序是:P>S>Na
c.基态As原子中,电子占据的最高能级为4d
d.Bi原子中最外层有5个能量相同的电子
(2)NH3在水中的溶解度比PH3大得多,其原因是___![]() 向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有___和___。
向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。该晶体中含有的化学键除普通的共价键外,还有___和___。
(3)PCl3分子中,Cl-P-Cl键的键角___109°28'(填“>”“<”或“2”![]() 。
。
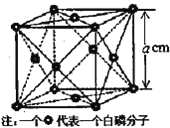
(4)白磷(P4)是磷的一种单质,它属于分子晶体,其晶胞结构如图。已知该晶体的密度为ρg·cm-3,晶胞的边长为acm,则阿伏加德罗常数为___mol-1(用含p、a的式子表示![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一反应:2A+B![]() 2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有 a、b、c三点,如图所示,则下列描述正确的是
2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有 a、b、c三点,如图所示,则下列描述正确的是
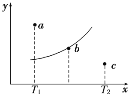
A.该反应是放热反应
B.b点时混合气体的平均摩尔质量不再变化
C.T1温度下若由a点达到平衡,可以采取增大压强的方法
D.c点:v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,密闭容器中充入一定物质的量的NO2 和SO2 ,发生如下反应: NO2+ SO2![]() NO + SO3 ,达到平衡时,下列叙述正确的是
NO + SO3 ,达到平衡时,下列叙述正确的是
A、 SO2 、NO2、NO、SO3 的物质的量一定相等
B、 NO2和 SO2 的物质的量一定相等
C、平衡体系中反应物的总物质的量一定等于生成物的总物质的量
D、NO 和 SO3 的物质的量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验制备Ca(NO2)2,实验装置如图所示(夹持装置已略去)。已知:2NO+CaO2==Ca(NO2)2;2NO2+CaO2==Ca(NO3)2。下列说法不正确的是

A. 通入N2是为了排尽装置中的空气
B. 装置B、D中的试剂可分别为水和浓硫酸
C. 将铜片换成木炭也可以制备纯净的亚硝酸钙
D. 借助装置A及氢氧化钠溶液和稀硫酸可以分离CO2和CO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com