
下列各溶液中,微粒的物质的量浓度关系正确的是( )
|
| A. | 10 mL 0.5 mol•L﹣1CH3COONa溶液与6 mL 1 mol•L﹣1盐酸混合:c(Cl﹣)>c(Na+)>c(OH﹣)>c(H+) |
|
| B. | 0.1 mol•L﹣1pH为4的NaHB溶液中:c(HB﹣)>c(H2B)>c(B2﹣) |
|
| C. | 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA﹣)+c(OH﹣)+c(A2﹣) |
|
| D. | 0.1 mol•L﹣1CH3COONa溶液中:c(OH﹣)=c(CH3COOH)+c(H+) |
考点:
离子浓度大小的比较;弱电解质在水溶液中的电离平衡;盐类水解的应用.
专题:
电离平衡与溶液的pH专题;盐类的水解专题.
分析:
A、依据化学方程式计算反应后溶液中的溶质成分,结合离子性质分析判断;
B、0.1 mol•L﹣1 依据PH=4,判断溶液为酸性,HB﹣判断为弱酸酸式酸根,依据电离大于水解分析;
C、依据溶液中电荷守恒计算分析;
D、依据溶液中质子守恒分析判断.
解答:
解:A、10 mL 0.5 mol•L﹣1CH3COONa溶液与6 mL 1 mol•L﹣1盐酸混合反应后溶液中0.005molCH3COONa、0.001molHCl,0.005molNaCl,溶液中c(Cl﹣)<c(Na+),c(OH﹣)<c(H+),故A 错误;
B、0.1 mol•L﹣1pH为4的NaHB溶液中,HB﹣判断为弱酸酸式酸根,电离大于水解,c(B2﹣)>c(HB﹣)>c(H2B),故B错误;
C、在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA﹣)+c(OH﹣)+2c(A2﹣),故C错误;
D、0.1 mol•L﹣1CH3COONa溶液中存在质子守恒得到:c(OH﹣)=c(CH3COOH)+c(H+),故D正确;
故选D.
点评:
本题考查了溶液中离子浓度大小比较,溶液中电荷守恒、质子守恒的应用,离子性质的判断,溶液酸碱性的分析,题目难度中等.


科目:高中化学 来源: 题型:
一定条件下合成乙烯。
6H2(g)+2CO2(g)  C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
 (1)乙烯是___________分子。(填极性或非极性)
(1)乙烯是___________分子。(填极性或非极性)
(2)请在方程式上标出该反应电子转移的方向和数目。
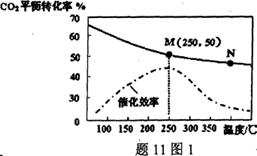
(3)温度对CO2的平衡转化率和催化剂催化效率的影
响如题11图1,下列说法正确的是___________。
A.此反应随温度升高,反应速率一定加快
B.平衡常数:KM>KN
C.M点CO2的平衡转化率受温度、催化剂的共同影响
 (4)若投料比n(H2):n(CO2)=3:1,图中M点乙烯的体积分数为___________ (保留两位有效数字)。
(4)若投料比n(H2):n(CO2)=3:1,图中M点乙烯的体积分数为___________ (保留两位有效数字)。
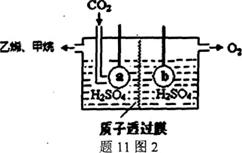
(5)电解法制取乙烯装置如题11图2,电极a接电源的
___________极,生成乙烯的电极反应式为___________。
当左侧有33.6L(标准状况)CO2反应时,左右两侧溶液
质量差|△m右|﹣|△m左|=36g,则乙烯的产率为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
|
| A. | 钠、钾着火时可用水灭火 |
|
| B. | 面粉厂或加油站不必严禁烟火 |
|
| C. | 氨气泄漏时可喷洒大量水进行处理 |
|
| D. | 节日期间可在人群聚集的闹市燃放烟花爆竹 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组比较中,前者比后者大的是( )
|
| A. | 25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度 |
|
| B. | 25℃时,pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度 |
|
| C. | 同温度、同浓度的NaCl溶液和氨水的导电能力 |
|
| D. | 25℃时,pH均为3的HCl和FeCl3溶液中水的电离程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分别取pH均等于2的盐酸和醋酸各l00mL,稀释2倍后,再分别加入足量锌粉,在相同条件下充分反应,下列有关叙述正确的是
( )
|
| A. | 反应开始时,盐酸和醋酸分别与锌反应的速率一样大 |
|
| B. | 反应开始时,盐酸与锌反应的速率大 |
|
| C. | 盐酸和醋酸分别与锌反应放出的氢气一样多 |
|
| D. | 醋酸与锌反应放出氢气多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请回答下列问题:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 .直到因加入一滴盐酸后,溶液由黄色变为橙色,并 为止.
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是 (填字母)
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面分别如图所示,则起始读数为 mL,终点读数为 mL;所用盐酸的体 mL.
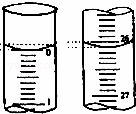
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子,在指定的环境中可能大量共存的是( )
|
| A. | 水电离出来的c(H+)=10﹣13mol/L的溶液:K+、HCO3﹣、Br﹣、Ba2+ |
|
| B. | 滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl﹣、NO3﹣ |
|
| C. | 与金属铝反应只能放出氢气的溶液:NO3﹣、K+、Cl﹣、Na+、OH﹣ |
|
| D. | c(H+)>c(OH﹣)的溶液中:Na+、K+、SO42﹣、S2﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C都是有机化合物,且有如下转化关系:A B
B C,A的相对分子质量比B大2,C的相对分子量比B大16,C能与过量的NaOH反应生成一种常见的气体,以下说法正确的是( )
C,A的相对分子质量比B大2,C的相对分子量比B大16,C能与过量的NaOH反应生成一种常见的气体,以下说法正确的是( )
|
| A. | A是乙炔,B是乙烯 | B. | A是乙烯,B是乙烷 |
|
| C. | A是乙醇,B是乙醛 | D. | A是环己烷,B是苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com