
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĀĮ¼°Ęä»ÆŗĻĪļµÄŠšŹöÕżČ·µÄŹĒ(””””)
A. ĀĮ·ŪÓėŃõ»ÆĢśŌŚøßĪĀĻĀæÉŅŌ·¢ÉśĀĮČČ·“Ó¦
B. µČĮæµÄĀĮ·Ö±šÓė×ćĮæµÄŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬²śÉśµÄĒāĘųĢå»ż²»Ķ¬
C. ¹¤ŅµÉĻÓƵē½āČŪČŚAlCl3µÄ·½·ØŅ±Į¶ĀĮ
D. ČżŃõ»Æ¶žĀĮŹĒĖįŠŌŃõ»ÆĪļ
”¾“š°ø”æA
”¾½āĪö”æA. ĀĮ·ŪÓėŃõ»ÆĢśŌŚøßĪĀĻĀæÉŅŌ·¢ÉśĀĮČČ·“Ӧɜ³ÉŃõ»ÆĀĮÓėĢś£¬AÕżČ·£»B. µČĮæµÄĀĮ·Ö±šÓė×ćĮæµÄŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬²śÉśµÄĒāĘųĢå»żĻąĶ¬£¬B“ķĪó£»C. ¹¤ŅµÉĻÓƵē½āČŪČŚŃõ»ÆĀĮAlCl3µÄ·½·ØŅ±Į¶ĀĮ£¬AlCl3ŌŚČŪȌדĢ¬ĻĀ²»ÄܵēĄė³öŅõŃōĄė×Ó£¬²»µ¼µē£¬C“ķĪó£»D. ČżŃõ»Æ¶žĀĮŹĒĮ½ŠŌŃõ»ÆĪļ£¬D“ķĪ󣬓š°øŃ”A”£


 ×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŖµÄµ„ÖŹ¼°Ņ»Š©»ÆŗĻĪļŌŚ¹¤Å©ŅµÉś²śµČĮģÓņÓŠÖŲŅŖ×÷ÓĆ£¬»Ų“šĻĀĮŠĪŹĢā
(1)NŌ×ÓŗĖĶāÓŠ________²»Ķ¬ŌĖ¶ÆדĢ¬µÄµē×Ó”£»łĢ¬NŌ×ÓÖŠ£¬ÄÜĮæ×īøߵĵē×ÓĖłÕ¼¾ŻµÄŌ×Ó¹ģµĄŠĪדĪŖ_____________________£»
(2)NÓėĶ¬Ņ»ÖÜĘŚÖŠ×óÓŅĻąĮŚµÄĮ½ÖÖŌŖĖŲŌ×ӵĵŚŅ»µēĄėÄܓ󊔹ŲĻµĪŖ______________(ĢīŌŖĖŲĆū³Ę)£¬øƵēĄėÄÜ“óŠ”±ä»ÆµÄŌŅņĪŖ______________________________________________£»
(3)¾²ā¶Ø·¢ĻÖ£¬N2O5¹ĢĢåÓÉNO2+ŗĶNO3£Į½ÖÖĄė×Ó×é³É£¬øĆ¹ĢĢåÖŠNŌ×ÓŌÓ»ÆĄąŠĶĪŖ____________________£»ÓėNO2+»„ĪŖµČµē×ÓĢåµÄĪ¢Į£ÓŠ_______________(Š“³öŅ»ÖÖ)”£
(4)ŗ¬µŖµÄijŠ©ÅäĢåæÉÓėCo3+ÅäĪ»£¬ĒėÅŠ¶ĻCoŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķÖŠµÄ____________Ēų(Ģīs”¢p”¢d”¢ds»ņf)£¬ŹŌŠ“³öøĆCoŌŖĖŲ»łĢ¬Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½________________________£»Co3+µÄŅ»ÖÖÅäĄė×Ó[Co(N3)(NH3)5]2+ÖŠ£¬Co3+µÄÅäĪ»ŹżĪŖ_______________”£ŅŃÖŖÅäĢåN3£ÓėCO2ĪŖµČµē×ÓĢ壬Ŋ¶ĻN3£µÄæÕ¼äĮ¢Ģå¹¹ŠĶĪŖ_____________________”£
(5)ŅŃÖŖNµÄµēøŗŠŌ“óÓŚCl£¬NCl3ÄÜÓėĖ®·¢Éś¾ēĮŅµÄĖ®½ā·“Ó¦£¬·“Ó¦µĆµ½Į½ÖÖøßÖŠ³£¼ūµÄ»ÆѧĪļÖŹ£¬Ōņ·¢ÉśµÄ»Æѧ·½³ĢŹ½ĪŖ_______________________________________________”£
(6)ÓÉH”¢C”¢N”¢OĖÄÖÖŌŖĖŲ¹²Ķ¬×é³ÉµÄĖÄŌ×Ó·Ö×Ó¾ßÓŠ¶ąÖÖ²»Ķ¬µÄ½į¹¹£¬ĒėŠ“³öĘäÖŠĮ½ÖÖĀś×ćĪČ¶Ø½į¹¹µÄĮ“דŅģ¹¹ĢåµÄµē×ÓŹ½____________________”¢______________________£»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
A. ŌŚNH![]() ŗĶ[Cu(NH3)4]2£«ÖŠ¶¼“ęŌŚÅäĪ»¼ü
ŗĶ[Cu(NH3)4]2£«ÖŠ¶¼“ęŌŚÅäĪ»¼ü
B. 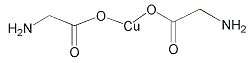 ¦Ņ¼üŗĶ¦Š¼ü±ČĄżĪŖ7:1
¦Ņ¼üŗĶ¦Š¼ü±ČĄżĪŖ7:1
C. C![]() ÓėO
ÓėO![]() »„ĪŖµČµē×ÓĢ壬1 mol O
»„ĪŖµČµē×ÓĢ壬1 mol O![]() ÖŠŗ¬ÓŠµÄ¦Š¼üŹżÄæĪŖ2NA
ÖŠŗ¬ÓŠµÄ¦Š¼üŹżÄæĪŖ2NA
D. ŅŃÖŖ·“Ó¦N2O4(l)£«2N2H4(l)===3N2(g)£«4H2O(l)£¬ČōøĆ·“Ó¦ÖŠÓŠ4 mol N”ŖH¼ü¶ĻĮŃ£¬ŌņŠĪ³ÉµÄ¦Š¼üŹżÄæĪŖ3NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪĀ¶ČĪŖT1Ź±£¬ŌŚČżøöČŻ»ż¾łĪŖ1 LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ½ö·¢Éś·“Ó¦£ŗ2NO2(g)![]() 2NO(g)+O2 (g) (Õż·“Ó¦ĪüČČ)”£ŹµŃé²āµĆ: vÕż= v(NO2)ĻūŗÄ=kÕżc2(NO2 )£¬vÄę= v(NO)ĻūŗÄ=2v(O2)ĻūŗÄ= kÄęc2 (NO)”¤c(O2 )£¬kÕż”¢kÄęĪŖĖŁĀŹ³£Źż£¬ŹÜĪĀ¶ČÓ°Ļģ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
2NO(g)+O2 (g) (Õż·“Ó¦ĪüČČ)”£ŹµŃé²āµĆ: vÕż= v(NO2)ĻūŗÄ=kÕżc2(NO2 )£¬vÄę= v(NO)ĻūŗÄ=2v(O2)ĻūŗÄ= kÄęc2 (NO)”¤c(O2 )£¬kÕż”¢kÄęĪŖĖŁĀŹ³£Źż£¬ŹÜĪĀ¶ČÓ°Ļģ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
ČŻĘ÷±ąŗÅ | ĪļÖŹµÄĘšŹ¼ÅضČ(mol”¤L-1) | ĪļÖŹµÄĘ½ŗāÅضČ(mol”¤L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
I | 0.6 | 0 | 0 | 0.2 |
II | 0.3 | 0.5 | 0.2 | |
¢ó | 0 | 0.5 | 0.35 | |
A. “ļĘ½ŗāŹ±£¬ČŻĘ÷IÓėČŻĘ÷¢ņÖŠµÄ×ÜŃ¹ĒæÖ®±ČĪŖ 4”Ć5
B. “ļĘ½ŗāŹ±£¬ČŻĘ÷ÖŠ¢ņÖŠ c(O2)/ c(NO2) ±ČČŻĘ÷IÖŠµÄ“ó
C. “ļĘ½ŗāŹ±£¬ČŻĘ÷¢óÖŠNOµÄĢå»ż·ÖŹżŠ”ÓŚ50%
D. µ±ĪĀ¶ČøıäĪŖ T2Ź±£¬Čō kÕż=kÄę£¬Ōņ T2<T1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25”ꏱ£¬ÓŠĻĀĮŠĖÄÖÖČÜŅŗ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
¢Ł | ¢Ś | ¢Ū | ¢Ü |
0.1mol/LµÄ°±Ė® | pH=11µÄ°±Ė® | 0.1mol/LµÄŃĪĖį | pH=3µÄŃĪĖį |
A£®¢ŁĻ”ŹĶµ½ŌĄ“µÄ100±¶ŗó£¬pHÓė¢ŚĻąĶ¬
B£®µČĢå»ż¢Ł¢Ū»ģŗĻ”¢µČĢå»ż¢Ś¢Ü»ģŗĻĖłµĆµÄČÜŅŗ¶¼³ÉĖįŠŌ
C£®¢Ł¢ŚÖŠ·Ö±š¼ÓČėÉŁĮæCH3COONa¹ĢĢ壬![]() µÄÖµ±äŠ”
µÄÖµ±äŠ”
D£®½«20mLµÄ¢ŁČÜŅŗÓė10mLµÄ¢ŪČÜŅŗ»ģŗĻŗó£¬ČōČÜŅŗ³Ź¼īŠŌ£¬Ōņc(NH4+)>c(Cl-)> c(NH3H2O)> c(OH-)>c(H+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĻĀĶ¼ĖłŹ¾£¬ŹŅĪĀĻĀµÄĮ½øöĮ¬ĶØøÕŠŌČŻĘ÷ÓĆ»īČū·ÖæŖ£¬×óÓŅĮ½ŹŅĢå»żĻąĶ¬£¬×óŹŅ³äČėŅ»¶ØĮæNO£¬ÓŅŹŅ³äČėŅ»¶ØĮæO2£¬ĒŅĒ”ŗĆŹ¹Į½ČŻĘ÷ÄŚĘųĢåĆܶČĻąĶ¬”£“ņæŖ»īČū£¬Ź¹NOÓėO2³ä·Ö·“Ó¦ĒŅ»Öø“ÖĮŹŅĪĀ£¬·“Ó¦ČēĻĀ:2NO+O2=2NO2”£²»æ¼ĀĒNO2×Ŗ»ÆĪŖN2O4£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
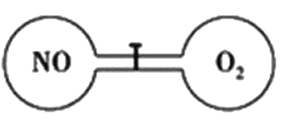
A. ·“Ó¦Ē°ŗó×óŹŅµÄŃ¹ĒæĻąĶ¬
B. ·“Ó¦ŗóČŻĘ÷ÄŚµÄĆܶČÓė·“Ó¦Ē°µÄĻąĶ¬
C. æŖŹ¼Ź±×óÓŅĮ½ŹŅÖŠµÄ·Ö×ÓŹżĻąĶ¬
D. ·“Ó¦ŗóČŻĘ÷ÄŚĪŽO2“ęŌŚ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĪĀ¶ČT1ŗĶT2Ź±£¬·Ö±š½«0.50 mol CH4ŗĶ1.20 mol NO2³äČėĢå»żĪŖ1 LµÄĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśČēĻĀ·“Ó¦£ŗCH4(g)£«2NO2(g)![]() N2(g)£«CO2(g)£«2H2O(g)£¬²āµĆn(CH4)Ėꏱ¼ä±ä»ÆŹż¾ŻČēĻĀ±ķ£ŗ
N2(g)£«CO2(g)£«2H2O(g)£¬²āµĆn(CH4)Ėꏱ¼ä±ä»ÆŹż¾ŻČēĻĀ±ķ£ŗ
Ź±¼ä/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | ”” | 0.15 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A. T1Ź±0”«10 min NO2µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.15 mol”¤L-1”¤min -1
B. T2Ź±CH4µÄĘ½ŗā×Ŗ»ÆĀŹĪŖ70.0%
C. ±£³ÖĘäĖūĢõ¼ž²»±ä£¬T1Ź±ĻņĘ½ŗāĢåĻµÖŠŌŁ³äČė0.30 mol CH4ŗĶ0.80 mol H2O(g)£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
D. ±£³ÖĘäĖūĢõ¼ž²»±ä£¬T1Ź±ĻņĘ½ŗāĢåĻµÖŠŌŁ³äČė0.50 mol CH4ŗĶ1.20 mol NO2£¬ÓėŌĘ½ŗāĻą±Č£¬“ļŠĀĘ½ŗāŹ±N2µÄÅضČŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
A. ±ź×¼×“æöĻĀ£¬0.1moLCl2ČÜÓŚĖ®£¬×ŖŅʵĵē×ÓŹżÄæĪŖ0.1NA
B. ±ź×¼×“æöĻĀ£¬22.4 L H2Oŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA
C. 1.8g D2Oŗ¬ÓŠµÄµē×ÓŹżĪŖ0.1NA
D. ³£ĪĀ³£Ń¹ĻĀ£¬1.06 g Na2CO3ŗ¬ÓŠµÄNa+ŹżĪŖ0.02NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·Ö±šÖ»ÓĆŅ»ÖÖŹŌ¼Į³żČ„ĻĀĮŠø÷×éÖŠĖłŗ¬µÄÉŁĮæŌÓÖŹ£ØĄØŗÅÄŚĪŖŌÓÖŹ£©£¬ŌŚæÕøńÖŠĢīÉĻŠč¼ÓČėµÄŅ»ÖÖŹŌ¼Į£ŗ
£Ø1£©FeCl3ČÜŅŗ£ØFeCl2£©________________”£
£Ø2£©FeCl2ČÜŅŗ£ØFeCl3£©________________”£
£Ø3£©Fe ·ŪÄ©£ØAl£© _______________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com