
 ;
;
| ||
| 冰晶石 |
 ;2Al2O3
;2Al2O3
| ||
| 冰晶石 |


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
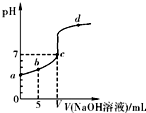 在25℃下,向10.00mL0.01mol?L-1某一元酸HA溶液中逐滴加入0,.01mol.L-1NaOH溶液,溶液pH变化曲线如图所示.下列说法正确的是( )
在25℃下,向10.00mL0.01mol?L-1某一元酸HA溶液中逐滴加入0,.01mol.L-1NaOH溶液,溶液pH变化曲线如图所示.下列说法正确的是( )| A、HA是强酸 |
| B、b点表示的溶液中:c(HA)=c(A-) |
| C、c点时:V=10.00mL |
| D、b、c、d三点表示的溶液中一定都存在:c(Na+)+c(H+)=c(A-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 | ||
| A | 向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH
| ||
| B | 将少量的溴水滴入FeCl2、NaI的混合溶液中,在滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液.再向上层溶液中滴加溴水 | 实验现象1: 上层溶液不变红 下层溶液紫色红 实验现象2: 上层溶液变红 | 氧化性:Br2>Fe3+>I2 | ||
| C | 淀粉在稀硫酸的作用下水解后,滴加NaOH溶液至碱性,再加入新制Cu(OH)2后加热 | 有砖红色沉淀生成 | 淀粉已经完全水解 | ||
| D | BaSO4固体加入饱和Na2CO3溶液中,过滤,箱滤渣中加入盐酸 | 有气体生成 | Ksp(BaCO3)<Ksp(BaSO4) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
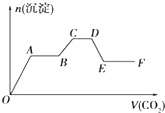 将CO2 气体缓缓通入到含有等物质的量的KOH、Ba(OH)2 和KAlO2 的混合溶液中,直至过量,生成的沉淀的物质的量与所通CO2 的体积关系如图所示(假设每步反应均完全).下列关于整个反应进程中的各种描述不正确的是( )
将CO2 气体缓缓通入到含有等物质的量的KOH、Ba(OH)2 和KAlO2 的混合溶液中,直至过量,生成的沉淀的物质的量与所通CO2 的体积关系如图所示(假设每步反应均完全).下列关于整个反应进程中的各种描述不正确的是( )| A、A→B段与C→D段所发生的反应相同 |
| B、B→C段反应的离子方程式是:2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32- |
| C、O→A段反应的化学方程式是:Ba(OH)2+CO2=BaCO3↓+H2O |
| D、D→E段沉淀的减少是由于碳酸钡固体的消失所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、工业制H2SO4时,催化氧化阶段的反应原理为2SO2+O2
| ||||
B、海水提镁的主要步骤为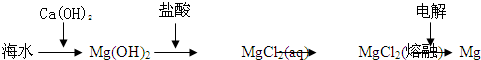 | ||||
C、冶炼铝时电解铝的反应原理为:2AlCl3
| ||||
D、高炉炼铁还原剂还原赤铁矿的化学方程式为:Fe2O3+3CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
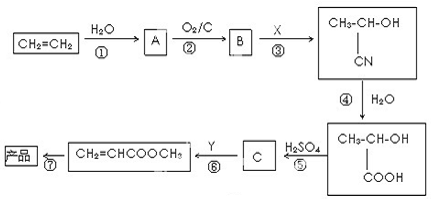
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100 mL0.1 mol?L-1的NaCl溶液 |
| B、50 mL 0.2 mol?L-1KCl溶液 |
| C、150 mL 0.15 mol?L-1的MgCl2溶液 |
| D、20 mL 0.5 mol?L-1FeCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com