
| A. | 乙醛 | B. | 丙醛 | C. | 丁醛 | D. | 戊醛 |
分析 选项中均为一元醛,结合-CHO~2Ag计算醛的物质的量,再结合完全燃烧时H原子守恒计算,以此来解答.
解答 解:由-CHO~2Ag可知,醛的物质的量为$\frac{21.6g}{108g/mol}$×$\frac{1}{2}$=0.1mol,
又等量的醛完全燃烧,生成3.6g H2O,n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,
由H原子守恒可知,醛中H原子个数为$\frac{0.2mol×2}{0.1}$=4,
则该醛为CH3CHO,为乙醛,
故选A.
点评 本题考查有机反应的计算,为高频考点,把握银镜反应中物质的量关系、原子守恒等为解答的关键,侧重分析与计算能力的考查,注意守恒法应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ④⑤⑥⑧ | B. | ④⑤⑦⑧ | C. | ③④⑤⑧ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 以葡萄糖为燃料的微生物燃料电池结构示意图如图所示. 关于该电池的叙述不正确的是( )
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示. 关于该电池的叙述不正确的是( )| A. | 该电池不能在高温下工作 | |
| B. | 电池右侧电极反应为:C6H12O6+6H2O-24e-=6CO2↑+24H+ | |
| C. | 放电过程中,H+通过质子交换膜向电池右侧迁移 | |
| D. | 在电池反应中,每消耗1mol氧气,理论上能生成CO2 22.4 L(标况) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60与金刚石一样属于原子晶体 | |
| B. | 水结冰体积膨胀、密度变小,这一事实与水分子间存在氢键有关 | |
| C. | 分子晶体中必含化学键 | |
| D. | 干冰升华破坏了共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
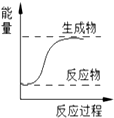
| A. | 金属钠与水的反应 | B. | 氢气燃烧 | ||
| C. | 浓硫酸的稀释 | D. | Ba(OH)2•8H2O和NH4Cl (固体)混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期元素的离子半径从左到右逐渐减小 | |
| B. | ⅥⅠA族元素的氢化物中,稳定性最好的沸点也最高 | |
| C. | 第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | |
| D. | 同周期非金属元素氧化物对应水化物的酸性从左到右依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com