
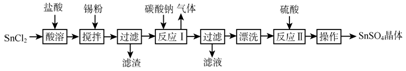
分析 为防止SnCl2水解,所以将SnCl2溶解在稀盐酸中,然后加入锡粉搅拌,防止Sn2+被氧化,然后过滤滤去滤渣,向滤液中加入碳酸钠,发生反应Sn2++CO32-═SnO↓+CO2↑,然后过滤得到滤渣,将滤渣洗涤,用硫酸溶解得到硫酸锡,将硫酸锡溶液蒸发浓缩、冷却结晶、干燥得到硫酸锡固体;
(1)由信息可知,SnCl2易水解生成碱式氯化亚锡,加入盐酸,抑制Sn2+水解;
(2)由信息可知,Sn2+易被氧化,加入Sn粉除调节溶液pH外,还防止Sn2+被氧化;
(3)在SnCl2的溶液中滴中纯碱溶液,生成SnO和CO2,结合原子守恒写出此反应的化学方程式;
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,双氧水有强氧化性,将Sn2+易被氧化为Sn4+,自身被还原为水;
(5)用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:6FeCl2+K2Cr2O7+14HCl═6FeCl3+2KCl+2CrCl3+7H2O,根据电子转移守恒与方程式可得关系式Sn~Sn2+~2Fe3+~2Fe2+~$\frac{1}{3}$K2Cr2O7,据此计算.
解答 解:(1)由信息可知,SnCl2易水解生成碱式氯化亚锡,存在平衡Sn Cl2+H2O?Sn(OH)Cl+HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解,
故答案为:SnCl2水解,发生SnCl2+H2O?Sn(OH)Cl+HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解;
(2)由信息可知,Sn2+易被氧化,加入Sn粉除调节溶液pH外,还防止Sn2+被氧化;
故答案为:防止Sn2+被氧化;
(3)反应Ⅰ是在SnCl2的溶液中滴中纯碱溶液,生成SnO和CO2,发生反应的化学方程式是:SnCl2+Na2CO3=SnO+CO2↑+2NaCl,故答案为:SnCl2+Na2CO3=SnO+CO2↑+2NaCl;
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,双氧水有强氧化性,将Sn2+易被氧化为Sn4+,自身被还原为水,离子方程式为:Sn2++H2O2+2H+═Sn4++2H2O,
故答案为:Sn2++H2O2+2H+═Sn4++2H2O;
(5)用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:6FeCl2+K2Cr2O7+14HCl═6FeCl3+2KCl+2CrCl3+7H2O,令锡粉中锡的质量分数为x,则存在
Sn~Sn2+~2Fe3+~2Fe2+~$\frac{1}{3}$K2Cr2O7;
119g $\frac{1}{3}$mol
1.130g×x 0.100mol/L×0.030L
故 $\frac{119g}{1.130xg}=\frac{\frac{1}{3}mol}{0.100mol/L×0.030L}$,解得x=94.78%,
故答案为:94.78%.
点评 本题以SnSO4的制备为载体,考查学生对工艺流程的理解、物质的分离提纯、阅读题目获取信息的能力、常用化学用语书写、滴定应用及利用关系式进行的计算等,难度中等,对学生的基础知识及逻辑推理有较高的要求.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
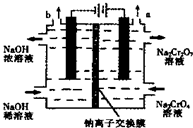 某工厂采用石墨电极电解Na2CrO4溶液,实现Na2CrO4到 Na2Cr2O7的转化,其装置如图所示.下列说法正确的是( )
某工厂采用石墨电极电解Na2CrO4溶液,实现Na2CrO4到 Na2Cr2O7的转化,其装置如图所示.下列说法正确的是( )| A. | 阳极区的pH会不断下降 | |
| B. | 溶液中Na+从阴极移向阳极 | |
| C. | 该电解池的两电极材料只能用石墨不能用铁 | |
| D. | 阳极区发生的反应是:2H2O-4e-═O2↑+4H+,2CrO42-+2H+═Cr2O72-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4[H2SO4] | B. | KBr[H2O] | C. | 盐酸[HCl] | D. | Cu(NO3)2[Cu(OH)2] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.2mol•L-1CH3COOH溶液中加入等体积0.1mol•L-1NaOH溶液,测得溶液中c(CH3COO-)>c(Na+),则水的电离程度比纯水的大 | |
| B. | 向0.1 mol•L-1氨水中滴加0.1 mol•L-1盐酸,刚好完全中和时溶液pH=a,则由水电离产生的c(OH-)=10a-14mol•L-1 | |
| C. | 将0.1 mol•L-1Na2CO3和0.1 mol•L-1NaHCO3溶液等体积混合,所得溶液有:c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c(H2CO3) | |
| D. | 对于难溶电解质:相同温度时,Ksp大的饱和溶液的物质的量浓度一定比Ksp小的饱和溶液物质的量浓度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 136g熔融的KHSO4中含有2NA个阳离子 | |
| B. | 40gH218O与40gD2O所含的中子数均为20NA | |
| C. | 1molFe分别与足量的稀硫酸和稀硝酸反应转移电子数均为2NA | |
| D. | 标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PH3 分子是非极性分子 | |
| B. | PH3分子中有一对电子孤对 | |
| C. | PH3 分子VSEPR模型的名称是四面体 | |
| D. | PH3 分子稳定性低于 NH3 分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色中性溶液中:Na+、K+、CO32-、SO42- | |
| B. | 含有大量Fe3+的溶液中:Na+、Mg2+、NO3-、I- | |
| C. | 加入铝粉后有气体放出的溶液:Fe2+、K+、NO3-、Cl- | |
| D. | 能使酚酞变红色的溶液:CO32-、Cl-、F-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com