
·ÖĪö £Ø1£©¹ĢĢå¼õÉŁµÄÖŹĮæĪŖ¶žŃõ»ÆĢ¼ŗĶĖ®µÄÖŹĮæÖ®ŗĶ£¬øł¾Ż·½³ĢŹ½¼ĘĖćĶĀĢµÄÖŹĮ棻
£Ø2£©39.2gĄ¶É«¹ĢĢåĪŖĒāŃõ»ÆĶ£¬øł¾ŻCuŌ×ÓŹŲŗć¼ĘĖćCuŌŖĖŲµÄÖŹĮ棬ŌŁĒó³öCuµÄÖŹĮæ·ÖŹż£»
£Ø3£©Éč¹ĢĢåÖŠCu2£ØOH£©2CO3µÄĪļÖŹµÄĮæĪŖxmol£¬CuµÄĪļÖŹµÄĮæĪŖymol£¬øł¾ŻĶŌ×ÓŹŲŗćŗĶŅŃÖŖÖŹĮæĮŠŹ½¼ĘĖć£»
£Ø4£©¢ŁCuÓėĻõĖį·“Ó¦£¬CuŹ§Č„µÄµē×ÓµÄĪļÖŹµÄĮæµČÓŚĘųĢåµĆµ½µÄµē×ÓµÄĪļÖŹµÄĮ棬¼ŁÉčֻɜ³ÉNOĒó³öĘųĢåµÄĢå»ż£¬»ņÕß¼ŁÉčֻɜ³ÉNO2ŌŁĒó³öĘųĢåµÄĢå»ż£¬Źµ¼ŹÉĻÉś³ÉµÄŹĒĮ½ÖÖĘųĢ壬ŌņĢå»żŌŚĮ½ÕßÖ®¼ä£»
¢Ś±ķĆęŅŃŠāŹ“³ÉĶĀĢ[Cu2£ØOH£©2CO3]µÄĶʬÓėĻõĖį·“Ӧɜ³ÉĻõĖįĶŗĶµŖµÄŃõ»ÆĪļ£¬ČÜŅŗÖŠ»¹ÓŠŹ£ÓąµÄĻõĖį£¬øł¾ŻµŖŌ×ÓŹŲŗć¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©¹ĢĢå¼õÉŁµÄÖŹĮæĪŖ¶žŃõ»ÆĢ¼ŗĶĖ®µÄÖŹĮæÖ®ŗĶ£¬Ōņ¶žŃõ»ÆĢ¼ŗĶĖ®µÄÖŹĮæÖ®ŗĶĪŖ9.3g£¬ÉčĶĀĢµÄÖŹĮæĪŖxg£¬
Cu2£ØOH£©2CO3 $\stackrel{”÷}{”ś}$2CuO+H2O+CO2”ü ¹ĢĢåÖŹĮæ±ä»Æ
222 62
xg 9.3g
Ōņx=$\frac{222”Į9.3}{62}$=33.3g
¹Ź“š°øĪŖ£ŗ33.3£»
£Ø2£©39.2gĄ¶É«¹ĢĢåĪŖĒāŃõ»ÆĶ£¬ŌņĒāŃõ»ÆĶÖŠCuŌŖĖŲµÄÖŹĮæĪŖ$\frac{39.2g”Į64}{98}$=25.6g£¬ŌņCuµÄÖŹĮæ·ÖŹżĪŖ$\frac{25.6g}{35g}$”Į100%=73.14%£»
¹Ź“š°øĪŖ£ŗ73.14%£»
£Ø3£©Éč¹ĢĢåÖŠCu2£ØOH£©2CO3µÄĪļÖŹµÄĮæĪŖxmol£¬CuµÄĪļÖŹµÄĮæĪŖymol£¬ŅŃÖŖĶĀĢŗĶĶµÄ×ÜÖŹĮæĪŖ35g£¬Éś³ÉĒāŃõ»ÆĶ³ĮµķµÄÖŹĮæĪŖ39.2g£¬
Ōņ$\left\{\begin{array}{l}{222x+64y=35g}\\{98£Ø2x+y£©=39.2g}\end{array}\right.$£¬½āµĆ£ŗx=0.1£¬y=0.2£¬
¹Ź“š°øĪŖ£ŗ0.2£»
£Ø4£©¢ŁCuÓėĻõĖį·“Ó¦£¬¼ŁÉčֻɜ³ÉNO£¬ÓÉ·½³ĢŹ½3Cu+8HNO3£ØĻ”£©ØT3Cu£ØNO3£©2+2NO”ü+4H2OæÉÖŖ£¬CuĪŖ0.2mol£¬ŌņNOĪŖ$\frac{0.4}{3}$mol£¬ĘäĢå»żĪŖ$\frac{0.4}{3}$mol”Į22.4L/mol=$\frac{8.96}{3}$L£¬
CuÓėĻõĖį·“Ó¦£¬¼ŁÉčֻɜ³ÉNO2£¬ÓÉ·½³ĢŹ½Cu+4HNO3=Cu£ØNO3£©2+2NO2”ü+2H2OæÉÖŖ£¬CuĪŖ0.2mol£¬ŌņNOĪŖ0.4mol£¬ĘäĢå»żĪŖ0.4mol”Į22.4L/mol=8.96L£¬
Źµ¼ŹÉĻÉś³ÉµÄŹĒĮ½ÖÖĘųĢ壬ŌņĢå»żŌŚĮ½ÕßÖ®¼ä£¬¼“$\frac{8.96}{3}$£¼a£¼8.96£»
“š£ŗaµÄȔֵ·¶Ī§ĪŖ$\frac{8.96}{3}$£¼a£¼8.96£»
¢Ś±ķĆęŅŃŠāŹ“³ÉĶĀĢ[Cu2£ØOH£©2CO3]µÄĶʬÓėĻõĖį·“Ӧɜ³ÉĻõĖįĶŗĶµŖµÄŃõ»ÆĪļ£¬ČÜŅŗÖŠ»¹ÓŠŹ£ÓąµÄĻõĖį£¬¼ÓNaOHČÜŅŗĻõĖįĶ×Ŗ»ÆĪŖĒāŃõ»ÆĶ³Įµķ£¬
Cu£ØOH£©2µÄĪļÖŹµÄĮæĪŖ$\frac{39.2g}{98g/mol}$=0.4mol£¬
Cu£ØNO3£©2”«”«Cu£ØOH£©2 ”«”«2HNO3
0.4mol 0.4mol 0.8mol
·“Ó¦ŗóČÜŅŗPHÖµĪŖ1£¬ČÜŅŗÖŠŹ£ÓąµÄĻõĖįĪŖ0.1mol/L”Į0.1L=0.01mol£¬
ĖłŅŌĻõĖįµÄ×ÜĪļÖŹµÄĮæĪŖ0.8mol+0.01mol+$\frac{a}{22.4}$mol£¬ĖłŅŌĻõĖįµÄÅضČĪŖ£Ø8.1+$\frac{a}{2.24}$£©mol/L£»
“š£ŗŌĻõĖįµÄĪļÖŹµÄĮæÅضČĪŖ£Ø8.1+$\frac{a}{2.24}$£©mol/L£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ¹Ų·½³ĢŹ½µÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬²ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦£¬×¢Ņā°ŃĪÕ¼«ĻŽ·ØŌŚ¼ĘĖćÖŠµÄÓ¦ÓĆ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 10gH2ŗĶ10gO2 | B£® | 11.2LN2£Ø±ź×¼×“æöĻĀ£©ŗĶ11gCO | ||
| C£® | 9gH2OŗĶ0.5mol Br2 | D£® | 224mlH2£Ø±ź×¼×“æöĻĀ£©ŗĶ0.1mol N2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
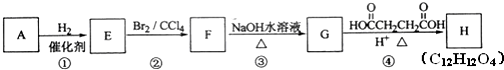
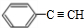 £¬Ćū³ĘŹĒ±½ŅŅČ²£»
£¬Ćū³ĘŹĒ±½ŅŅČ²£»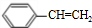 +Br2”ś
+Br2”ś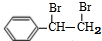 £»
£»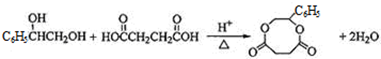 £»
£» £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹żĮæµÄNaHSO4ŗĶBa£ØOH£©2ČÜŅŗ·“Ó¦£ŗH++SO42-+Ba2++OH-ØTBaSO4”ż+H2O | |
| B£® | NaHCO3ŗĶ¹żĮæNaOHČÜŅŗĻą»ģŗĻ£ŗHCO3-+OH-ØTCO32-+H2O | |
| C£® | NaHSO4ČÜŅŗÖŠµĪ¼ÓNaHCO3ČÜŅŗ£ŗH++HCO3-ØTH2O+CO2”ü | |
| D£® | ÓĆNaOHĪüŹÕ¹żĮæµÄCO2£ŗCO2+OH-ØTHCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆFeCl3ČÜŅŗøÆŹ“ĶĻßĀ·°å£ŗFe3++3CuØTFe2++3Cu2+ | |
| B£® | ÉŁĮæ°±ĘųÖŠĶØČė¹żĮæŃĒĮņĖįČÜŅŗÖŠ£ŗNH3+H2SO3ØTNH4++HSO3- | |
| C£® | Cl2ÓėĖ®·“Ӧɜ³ÉŃĪĖįŗĶ“ĪĀČĖį£ŗCl2+H2OØTH++Cl-+HClO | |
| D£® | Š”ĖÕ“ņČÜŅŗÖŠ¼ÓČė¹żĮæµÄÉÕ¼īČÜŅŗ£ŗHCO3-+OH-ØTCO32-+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŃČܽāµÄČÜÖŹŗĶĪ“ČܽāµÄČÜÖŹÖŹĮæĻąµČ | |
| B£® | ČÜÖŹ²»ŌŁČܽā£¬Ņņ“Ė“Ó±ķĆęæ“ČÜÖŹ²»ŌŁ¼õÉŁ£¬Ņ²²»ŌŁŌö¼Ó | |
| C£® | ÉżøßĪĀ¶Č£¬±„ŗĶČÜŅŗ½«±äĪŖ²»±„ŗĶČÜŅŗ | |
| D£® | ČÜÖŹµÄČܽāŗĶ½į¾§¼ĢŠų½ųŠŠ£¬ĒŅĖŁĀŹĻąµČ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com