
| A、2 Na2O2+2H2O═4NaOH+O2↑ |
| B、Na2O2+MnO2═Na2MnO4 |
| C、2 Na2O2+2H2SO4═2Na2SO4+2H2O+O2↑ |
| D、5 Na2O2+2KMnO4+8 H2SO4═2Na2SO4+K2SO4+MnSO4+8H2O+5O2↑ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L的甲酸溶液中c(H+)约为1×10-2 mol/L |
| B、甲酸能与水以任意比例互溶 |
| C、1mol/L的甲酸溶液10mL恰好与10mL1mol/L的NaOH溶液完全反应 |
| D、甲酸溶液的导电性比盐酸弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H>0△S>0 |
| B、△H<0△S<0 |
| C、△H<0△S>0 |
| D、△H>0△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
A、质子数为53、中子数为78的碘原子:
| ||
B、S2-的结构示意图: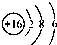 | ||
C、N2的电子式: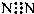 | ||
D、NH4I的电子式: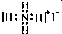 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向NaOH溶液中慢慢滴加FeCl3饱和溶液,可制得Fe(OH)3胶体 |
| B、胶体与其他分散系的本质区别是胶体能发生丁达尔效应 |
| C、除去Fe(OH)3胶体中的Na+和Cl-可用过滤的方法 |
| D、Fe(OH)3胶体中逐滴加入稀硫酸,会产生沉淀而后沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol 硫酸钾中阴离子所带电荷数为NA |
| B、标准状况下,NA个CCl4分子所占的体积约为22.4 L |
| C、将0.1mol氯化铁溶于1L水中,所得溶液中含有0.1NAFe3+ |
| D、常温常压下,16g O2和O3混合物中所含的O原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl-、NO3-、Al3+、Na+、 |
| B、Fe3+、Na+、SO42-、Cl- |
| C、Ba2+、Na+、NO3-、Cl- |
| D、Na+、K+、CO32-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com