
| A、XY |
| B、XY2 |
| C、X2Y |
| D、X2Y3 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠与水反应:Na+2H20=Na++20H一+H2↑ | ||
B、碳酸氢钠与盐酸反应:CO
| ||
| C、铁与稀硫酸反应:Fe+2H+=Fe3++H2↑ | ||
| D、醋酸溶液与氢氧化钠溶液反应:CH3COOH+OH一=CH3C00一+H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若在阴极附近的溶液中滴入酚酞试液,溶液呈无色 |
| B、若在阳极附近的溶液中滴入KI溶液,溶液呈棕色 |
| C、电解时在阳极得到氯气,在阴极得到金属钠 |
| D、电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酒精灯失火后,立即用水扑灭 |
| B、金属钠失火,立即用泡沫灭火器灭火 |
| C、苯酚沾在手上,立即用氢氧化钠溶液洗涤 |
| D、不慎将碱溅到皮肤上,立即用水冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、OH-、Na+ |
| B、K+、NO3-、Cu2+ |
| C、Ba2+、SO42-、Na+ |
| D、Fe3+、OH-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| n(H2) |
| n(CO2) |
| n(H2) |
| n(CO2) |
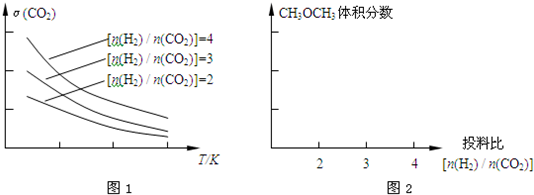
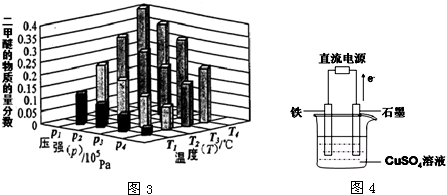
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com