
 电解饱和食盐水制取氯气和烧碱(氯碱工业)
电解饱和食盐水制取氯气和烧碱(氯碱工业)分析 根据电解池的工作原理,在阳极上是氯离子失电子生成氯气,在阴极上生成氢气和氢氧化钠,氯气具有氧化性,能使湿润的淀粉碘化钾显示蓝色,据此回答判断.
解答 解:根据电解池的工作原理,在阳极上是氯离子失电子生成氯气,在阴极上生成氢气和氢氧化钠,总反应为:
2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,氯气具有氧化性,能使湿润的淀粉碘化钾显示蓝色,检验的方法:用湿润的淀粉KI试纸检验气体,如果变蓝色,说明是氯气.
故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;用湿润的淀粉KI试纸检验气体,如果变蓝色,说明是氯气.
点评 本题考查学生电解池的工作原理以及氯气的性质知识,属于基本知识的考查,难度中等.


 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:解答题
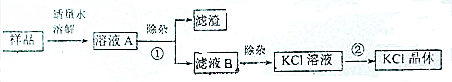
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉的有效成分是Ca(ClO)2和CaCl2 | |
| B. | 漂白粉在空气中久置后会变质 | |
| C. | 漂白粉的有效成分Ca(ClO)2不稳定,易分解 | |
| D. | 漂白粉的主要成分是CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.15 mol/L•min | B. | v(H2)=0.1 mol/L•min | ||
| C. | v(N2)=0.1 mol/L•min | D. | v(N2)=0.002 mol/L•s |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①②③④ | C. | ③④⑤ | D. | 全部都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 置换反应的通式可表示为如图所示:请回答下列问题:
置换反应的通式可表示为如图所示:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn与稀H2SO4反应:Zn+H+═Zn2++H2↑ | |
| B. | Na2CO3溶液与足量盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| C. | Cl2与NaOH溶液反应:Cl2+2OH-═2Cl-+H2O | |
| D. | MgCl2溶液与过量氨水反应:Mg2++2OH-═Mg(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
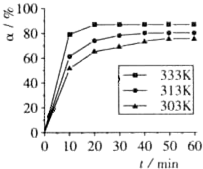
| A. | △H<0 | B. | △H>0 | C. | △H=0 | D. | 无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com