
| A. | 形成碳链 | B. | 形成碳环 | C. | 通过离子键 | D. | 通过共价键 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

 ,F
,F .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cu2+、Cl-、AlO2- | B. | Na+、Al3+、NO3-、HCO3- | ||
| C. | Na+、H+、NO3-、SO42- | D. | Ca2+、Cl-、CO32-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合物里三种物质反应时消耗盐酸的物质的量之比为1:1:3 | |
| B. | 反应后所得溶液中的Fe2+离子与Cl-离子的物质的量之比为1:2 | |
| C. | 混合物里,FeO的物质的量无法确定,但Fe和Fe2O3的物质的量一样多 | |
| D. | 混合物里,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
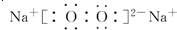 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 营养素 | 每100g含有 |
| 蛋白质 | 4.8g |
| 油脂 | 20g |
| 糖类 | 40g |
| -胡萝卜素 (维生素类) | 1.8g |
| 碳酸钙 | 400mg |
| A. | 油脂是高级脂肪酸的甘油酯 | |
| B. | 糖类是产生能量最高的营养物质 | |
| C. | 糖类、油脂、蛋白质都是高分子化合物 | |
| D. | 蛋白质在人体内水解最终生成二氧化碳和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用CO表示反应速率 | B. | 平衡混合气体的平均相对分子质量 | ||
| C. | CO的转化率 | D. | CO2的体积分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
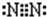 ,画出C元素的原子结构示意图
,画出C元素的原子结构示意图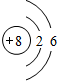 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com