
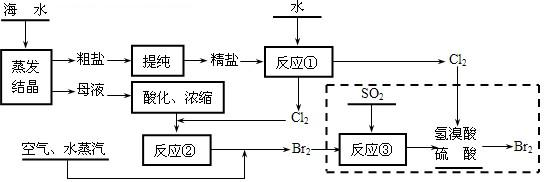
海洋约占地球表面积的71%,具有十分巨大的开发潜力。某校研究性学习小组同学对经初步净化处理的浓缩海水(主要含NaCl和MgSO4)进行研究。
(1)实验时,若配制1000 mL 0.20 mol/L NaOH溶液,计算称量固体NaOH的质量。
(2)取初步净化处理的浓缩海水100 mL,加入200 mL 0.20 mol/L NaOH溶液,恰好将其中的Mg2+完全沉淀,求浓缩海水中Mg2+的物质的量浓度。
(3)研究小组同学把上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解(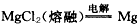 +Cl2) ,可得标准状况下Cl2多少升?
+Cl2) ,可得标准状况下Cl2多少升?
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
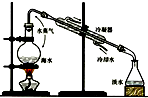
| 催化剂 |
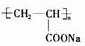
| 催化剂 |
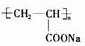
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
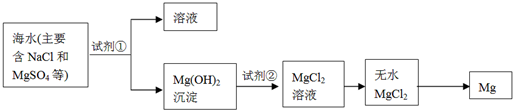
| △ |
| ||
| 2800℃ |
| △ |
| ||
| 还原 |
| HCl |
| ||
| 714℃ |
| HCl |
| ||
| 还原 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| △ |
| 电解 |
| 2800℃ |
| △ |
| C |
| 还原 |
| HCl |
| ||
| 714℃ |
| HCl |
| 活泼金属 |
| 还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
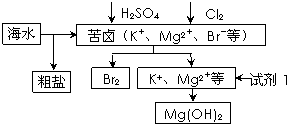
| A、可用BaCl2溶液除去粗盐中的SO42- | B、从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2═2Cl-+Br2 | C、试剂1可以选用石灰乳 | D、工业上,电解熔融MgO冶炼金属镁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com