
【题目】二乙酸![]() 环己二醇酯可通过下列路线合成:
环己二醇酯可通过下列路线合成:

(1)属于取代反应的是______,属于加成反应的是______(填序号).
(2)A的结构简式为______.
(3)写出反应④、⑦的化学方程式:______、______.
【答案】①⑥⑦ ③⑤⑧ 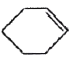
![]()
![]()
![]()
![]()

![]()
【解析】
环己烷与氯气在光照,发生取代反应产生一氯环己烷,一氯环己烷与NaOH的乙醇溶液在加热,发生消去反应产生A:环己烯![]() ;环己烯与溴的CCl4溶液,发生加成反应产生B:1,2-二溴环己烷;1,2-二溴环己烷与NaOH的乙醇溶液在加热,发生消去反应产生环己二烯
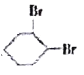
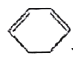
;环己烯与溴的CCl4溶液,发生加成反应产生B:1,2-二溴环己烷;1,2-二溴环己烷与NaOH的乙醇溶液在加热,发生消去反应产生环己二烯![]() ;
;![]() 与Br2按照1:1的物质的量的比发生1,4-加成产生
与Br2按照1:1的物质的量的比发生1,4-加成产生![]() ;
;![]() 与与NaOH溶液发生取代反应生成C:
与与NaOH溶液发生取代反应生成C: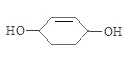 ;C与CH3COOH浓硫酸作用下发生酯化反应生成 D:
;C与CH3COOH浓硫酸作用下发生酯化反应生成 D:![]() 和水, D与氢气发生加成反应
和水, D与氢气发生加成反应![]() 。
。
(1)有分析可知:上述反应中,属于取代反应的有:①⑥⑦,属于加成反应的有:③⑤⑧;
本题答案为:①⑥⑦,③⑤⑧。
(2)A由一氯环己烷与NaOH的乙醇溶液在加热,发生消去反应产生的所以A为环己烯,结构简式为:![]() ;
;
本题答案为:![]() 。
。
(3)反应④是1,2-二溴环己烷与NaOH的乙醇溶液在加热,发生消去反应产生环己二烯![]() ,反应的化学方程式为:
,反应的化学方程式为:![]()
![]() 2NaOH
2NaOH![]()
![]()
![]() 2NaOH
2NaOH![]() 2H2O,反应⑦是
2H2O,反应⑦是 在浓硫酸作用下和醋酸发生的酯化反应,反应方程式为:
在浓硫酸作用下和醋酸发生的酯化反应,反应方程式为:
![]() 2CH3COOH
2CH3COOH![]()
![]()
![]() 2H2O;
2H2O;
本题答案为:![]()
![]() 2NaOH
2NaOH![]()
![]()
![]() 2NaOH
2NaOH![]() 2H2O,
2H2O,
![]() 2CH3COOH
2CH3COOH![]()
![]()
![]() 2H2O;
2H2O;


科目:高中化学 来源: 题型:
【题目】下列实验操作均要用玻璃棒,其中玻璃棒的作用相同的是:
①过滤 ②蒸发 ③溶解 ④向容量瓶转移溶液
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,有甲、乙两个密闭容器,甲容器的体积为1 L,乙容器的体积为2 L,分别向甲乙两容器中加入6 mol A和3 mol B,发生反应如下:3A(g)+bB(g)![]() 3C(g)+2D(g) ΔH<0,4 min时甲容器内的反应恰好达到平衡,A的浓度为2.4 mol·L-1,B的浓度为1.8 mol·L-1;t min时乙容器内的反应达到平衡,B的浓度为0.8 mol·L-1。根据题给信息回答下列问题:
3C(g)+2D(g) ΔH<0,4 min时甲容器内的反应恰好达到平衡,A的浓度为2.4 mol·L-1,B的浓度为1.8 mol·L-1;t min时乙容器内的反应达到平衡,B的浓度为0.8 mol·L-1。根据题给信息回答下列问题:
(1)甲容器中反应的平均速率v(B)=_______________,化学方程式中计量数b=_________。
(2)乙容器中反应达到平衡所需时间t_______4 min(填“大于”“小于”或“等于”),原因是___________________________________________________。
(3)T ℃时,在另一个体积与乙相同的丙容器中,为了达到平衡时B的浓度仍然为0.8 mol·L-1,起始时,向丙容器中加入C、D的物质的量分别为3 mol、2 mol,则还需加入A、B的物质的量分别是__________、__________。
(4)若要使甲、乙容器中B的平衡浓度相等,可以采取的措施是________。
A.保持温度不变,增大甲容器的体积至2 L
B.保持容器体积不变,使甲容器升高温度
C.保持容器压强和温度都不变,向甲中加入一定量的A气体
D.保持容器压强和温度都不变,向甲中加入一定量的B气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氧化性![]() .现有一包铁粉和铜粉混合粉末,某实验小组为了确定其组成,利用
.现有一包铁粉和铜粉混合粉末,某实验小组为了确定其组成,利用![]() 的
的![]() 溶液(其他用品略),与混合粉末反应,实验结果如下(假定反应前后溶液体积不变):
溶液(其他用品略),与混合粉末反应,实验结果如下(假定反应前后溶液体积不变):
组别 | ① | ② | ③ | ④ |
| 50 | 50 | 50 | 50 |
混合粉末质量/ | 1.2 | 2.4 | 3.6 | 4.8 |
反应后剩余固体质量/ | 0 | 0.64 | 1.92 | 3.12 |
分析表中数据,下列结论不正确的是
A. 第①组反应后溶液中剩余![]()
B. 第②、③组剩余固体全是铜
C. 第④组的滤液中![]()
D. 原混合粉末中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知固体甲为非金属,I、F均为常见的金属,E为气体单质;固体乙为一种红棕色固体;G为白色胶状沉淀,既能溶解于盐酸,又能溶解于氢氧化钠溶液.A在常温下为气态,与氧气完全反应时的体积比是![]() .W是由三种处在不同短周期的元素组成的化合物,与水反应生成A和G时的化学计量数之比为
.W是由三种处在不同短周期的元素组成的化合物,与水反应生成A和G时的化学计量数之比为![]() .各物质有如下图所示的转化关系(部分反应的产物未全部表示).试回答下列题:
.各物质有如下图所示的转化关系(部分反应的产物未全部表示).试回答下列题:

(1)B的电子式为______,固体甲、乙的化学式分别是______、______;
(2)上述转化中,①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]() ⑥
⑥![]() 其中属于置换反应的是(填序号)______;
其中属于置换反应的是(填序号)______;
(3)写出W和水反应的化学方程式______,![]() 和
和![]() 溶液反应的离子方程式______.
溶液反应的离子方程式______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为发光二极管连接柠檬电池装置,下列说法正确的是
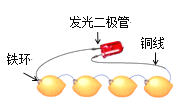
A. 铁环作为柠檬电池的正极
B. 电子由发光二极管经导线流向Fe环
C. 负极的电极反应为:Fe-2 e-===Fe2+
D. 可将柠檬替换成盛装酒精溶液的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法不正确的是
A. 0.2mol/L的NaHCO3溶液中: c(Na+)>c(HCO3-)>c(OH-)>c(H+)
B. 叠氮酸(HN3)与醋酸酸性相近,0.1mol/LNaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+)
C. 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中c(NH4+)=c(Cl-)
D. 0.02mol/L的NaOH溶液与0.04mol/L的NaHC2O4溶液等体积混合液:2c(OH-)+c(C2O42-)= c(HC2O4-)+2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组按如下实验过程证明了海带中存在碘元素:

下列说法不正确的是
A. 步骤①需要将干海带放入蒸发皿中灼烧
B. 步骤②中发生反应的离子方程式为2I-+2H++H2O2=I2+2H2O
C. 步骤③操作后,观察到试管中的溶液变为蓝色,则可说明海带中含有碘元素
D. 若步骤②仅滴加稀硫酸后通入氧气,则步骤③操作后,试管中的溶液也变成蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当温度高于500 K时,科学家成功利用二氧化碳和氢气合成了乙醇(可逆反应),这在节能减排、降低碳排放方面具有重大意义。回答下列问题:
(1)该反应的化学方程式______________________________________________。
(2)在恒容密闭容器中,判断上述反应达到平衡状态的依据是________。
a.体系压强不再改变
b.H2的浓度不再改变
c.气体的密度不随时间改变
d.单位时间内消耗H2和CO2的物质的量之比为3:1
(3)在一定压强下,测得由CO2制取CH3CH2OH的实验数据中,起始投料比、温度与CO2的转化率的关系如图。

根据图中数据
①降低温度,平衡向________方向移动。
②在700 K、起始投料比![]() =1.5时,H2的转化率为________。
=1.5时,H2的转化率为________。
③在500 K、起始投料比![]() =2时,达到平衡后H2的浓度为a mol·L-1,则达到平衡时CH3CH2OH的浓度为________。
=2时,达到平衡后H2的浓度为a mol·L-1,则达到平衡时CH3CH2OH的浓度为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com