
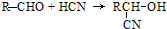
 ;扁桃酸
;扁桃酸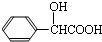 .
. .
. .
.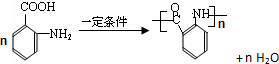 .
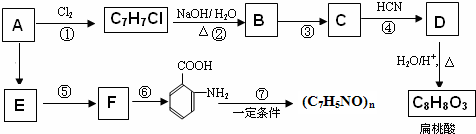
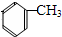
. 分析 芳香烃A与氯气反应生成氯代烃,由氯代烃的分子式可知应发生取代反应,故A分子式为C7H8,则A为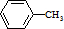 ,氯代烃水解生成B,B反应生成C,C和HCN发生信息I的反应,说明C中含有醛基,为
,氯代烃水解生成B,B反应生成C,C和HCN发生信息I的反应,说明C中含有醛基,为 ,B为
,B为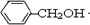 ,D为
,D为 ,D酸化得到扁桃酸,结构简式为
,D酸化得到扁桃酸,结构简式为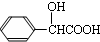 ,F发生反应信息Ⅲ的反应生成
,F发生反应信息Ⅲ的反应生成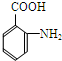 ,故F为
,故F为 ,结合转化关系可知,E为
,结合转化关系可知,E为 ,
, 发生缩聚反应生成
发生缩聚反应生成 ,据此分析解答.
,据此分析解答.
解答 解:芳香烃A与氯气反应生成氯代烃,由氯代烃的分子式可知应发生取代反应,故A分子式为C7H8,则A为 ,氯代烃水解生成B,B反应生成C,C和HCN发生信息I的反应,说明C中含有醛基,为
,氯代烃水解生成B,B反应生成C,C和HCN发生信息I的反应,说明C中含有醛基,为 ,B为
,B为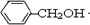 ,D为
,D为 ,D酸化得到扁桃酸,结构简式为
,D酸化得到扁桃酸,结构简式为 ,F发生反应信息Ⅲ的反应生成
,F发生反应信息Ⅲ的反应生成 ,故F为
,故F为 ,结合转化关系可知,E为
,结合转化关系可知,E为 ,
, 发生缩聚反应生成
发生缩聚反应生成 ,
,
(1)通过以上分析知,反应③为醇的催化氧化,反应条件是Cu、加热,反应④的类型是加成反应,
故答案为:Cu/加热; 加成反应;
(2)A的结构简式为 ,扁桃酸的结构简式为
,扁桃酸的结构简式为 ,故答案为:
,故答案为: ;
; ;
;
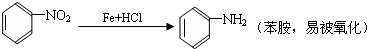
(3)如果对换,氨基将被氧化,所以不能对换,故答案为:氨基易被氧化,所以不能对换;
(4)该反应方程式为 ,故答案为:
,故答案为: ;
;
(5)该反应方程式为 ,故答案为:
,故答案为: ;
;
(6)该反应方程式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及信息迁移能力,明确反应前后结构变化及题给信息的灵活应用是解本题关键,注意醛基和HCN发生加成反应断键和成键位置,为易错点.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下使氢成为二次能源 | |
| B. | 寻找优质催化剂,使CO2与H2O反应生成CH4和O2,并放出热量 | |
| C. | 寻找优质催化剂,利用太阳能使大气中的CO2和海底开采的CH4合成合成气(CO、H2) | |
| D. | 将固态碳合成C60,以C60作燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸比磷酸易挥发 | |
| B. | 金刚石的熔点比晶体硅高 | |
| C. | 惰性气体一般很难发生化学反应 | |
| D. | 通常情况下单质溴呈液态、碘呈固态 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 实验过程中水的电离程度的变化是先增大后减小 | |
| B. | 当溶液呈中性时,反应恰好完全 | |
| C. | 当反应恰好完全时,消耗NaOH溶液10mL | |
| D. | 当溶液呈碱性时,其中离子浓度由大到小的顺序可能为c(Na+)>c(OH-)>c(Ac-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
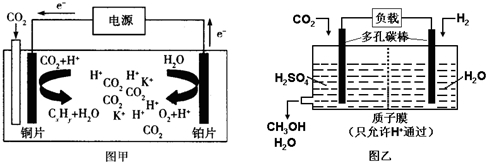
| A. | 甲中铜片作阴极,K+向铜片电极移动 | |
| B. | 甲中若CxHy为C2H4,则生成1mol C2H4的同时生成3mol O2 | |
| C. | 乙中H2SO4的作用是增强溶液的导电性 | |
| D. | 乙中正极发生的电极反应为CO2+5e-+6H+═CH3OH+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
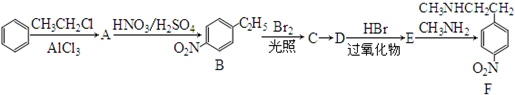
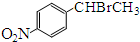 .
.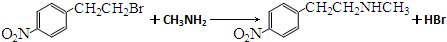 .
.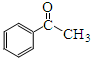 )常用作有机化学合成的中间体,参照上述合成F的部分步骤,设计一条以苯为起始原料制备苯乙酮的合成路线
)常用作有机化学合成的中间体,参照上述合成F的部分步骤,设计一条以苯为起始原料制备苯乙酮的合成路线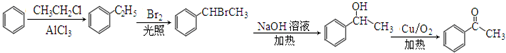 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
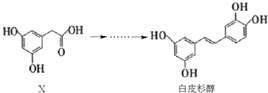
| A. | X的分子式为C8H10O4 | |
| B. | 化合物X、白皮杉醇均可与Na2CO3溶液反应并放出气体 | |
| C. | 白皮杉醇与浓溴水反应时,最多可消耗6 mol Br2 | |
| D. | 在一定条件下,白皮杉醇可发生加成、取代、氧化和聚合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 实验操作 | 实验目的 |
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
| C | 测定Na2CO3、Na2SO4两溶液的pH | 比较碳、硫的非金属性强弱 |
| D | 用同一电路测定等浓度的盐酸、醋酸两溶液的导电性 | 比较盐酸、醋酸的酸性强弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com