
【题目】一定条件下的密闭容器中:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述正确的是
4NO(g)+6H2O(g) ΔH=-905.9 kJ·mol-1,下列叙述正确的是
A. 平衡后升高温度,混合气体中NO含量增大
B. 平衡后降低压强,混合气体平均摩尔质量增大
C. 4molNH3和5molO2反应,达到平衡时放出热量为905.9kJ
D. 平衡时,将水蒸气移除部分,此时逆反应速率降低,正反应速率不变
科目:高中化学 来源: 题型:
【题目】甘油是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1.26g/mL,沸点约290℃,分离水和甘油最合理的方法是( )
A. 蒸馏 B. 蒸发 C. 过滤 D. 分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用资源,加强环境保护,降低碳排放,实施低碳经济是今后经济生活主流。回答下列问题:
(1)下列措施不利于有效减少二氧化碳的是_______(填字母)。
a.植树造林,保护森林,保护植被
b.加大对煤和石油的开采,并鼓励使用液化石油气
c.大力发展风能、水力、潮汐能发电和核电,大力推行太阳能的综合开发
d.推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
(2)科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以1:4的物质的量之比混合通入反应器,在适当条件下反应可获得一种重要能源。请完成以下化学方程式:
CO2+4H2![]() _______+2H2O
_______+2H2O
(3)用CO2合成燃料甲醇(CH3OH)是碳减排的新方向。现进行如下实验:某温度下在体积为1L的密闭容器中,充入2 mol CO2和6 mol H2,发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),能判断该反应已达化学平衡的标志是____(填字母)。
CH3OH(g)+H2O(g),能判断该反应已达化学平衡的标志是____(填字母)。
a.CO2百分含量保持不变
b.容器中混合气体的质量保持不变
c.容器中H2浓度与CO2浓度之比为3:1
d.CO2的生成速率与CH3OH的生成速率相等
现测得CO2相CH3OH (g)的浓度随时间变化如图所示。
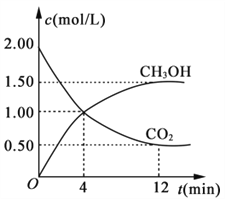
从反应开始到平衡,氢气的平均反应速率v(H2)=________。
(4)以KOH为电解质的甲醇燃料电池总反应为2CH3OH+3O2+4KOH=2K2 CO3+6H2O。通入甲醇的电极为燃料电池的______(填“正”或“负”)极,正极反应式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列保存试剂的方法中,错误的是( )
A.漂粉精保存在烧杯中B.新制的氯水保存在棕色瓶中,避光
C.氢氧化钠溶液保存在带木塞的试剂瓶D.碘单质保存在棕色瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
①3He和4He是同位素 ②金属性:K>Ca>Mg>Be
③四氯化碳的电子式:![]() ④离子键就是阴、阳离子的静电引力
④离子键就是阴、阳离子的静电引力
⑤通常活泼金属与活泼非金属元素形成离子化合物
⑥NaHSO4在熔融状态下电离,破坏了离子键和共价键
⑦用电子式表示溴化氢的形成过程为:![]()
A. ①④⑥ B. ④⑤⑥ C. ③④⑥⑦ D. 全部都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.物质在溶解时,若达到饱和状态,则该物质不再溶解
B.晶体失去结晶水,一定是风化的结果
C.从饱和溶液中结晶析出的晶体都含有结晶水
D.某饱和溶液冷却而析出晶体后,该溶液仍为饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各元素的原子或离子,各电子层都达到稳定结构的是( )
A.He、Ne、Ar、CaB.Be、B、C、Si
C.F、Cl、S、OD.Na+、F-、Cl-、Al3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com