
| 混合后的溶液 | 加入的酸 | 酸的浓度/(mol•L-1) | 混合后溶液的pH |
| ① | HA | 0.10 | 8.7 |
| ② | HB | 0.12 | 2 |
| A. | HA是强酸,HB是弱酸 | |
| B. | 升高温度,溶液②中$\frac{c({B}^{-})}{c(N{a}^{+})}$增大 | |
| C. | 溶液①中离子浓度的关系:c(A-)>c(Na+)>c(OH-)>c(H+) | |
| D. | 溶液②中离子浓度的关系:c(Na+)+c(H+)+c(B-)=0.12 mol•L-1 |
分析 0.10mol/L的HA与0.10mol•L-1的NaOH溶液等体积混合,恰好完全反应生成NaA,溶液的pH=8.7,显碱性,说明NaA为强碱弱酸盐,即HA为弱酸;
0.12mol/L的HB与0.10mol•L-1的NaOH溶液等体积混合,反应后剩余的酸的浓度为c(HB)=$\frac{0.12×V-0.1×V}{2V}$=0.01mol/L,溶液中c(H+)=0.01mol/l,所以HB完全电离,即NB为强酸,结合电荷守恒和物料守恒分析.
解答 解:0.10mol/L的HA与0.10mol•L-1的NaOH溶液等体积混合,恰好完全反应生成NaA,溶液的pH=8.7,显碱性,说明NaA为强碱弱酸盐,即HA为弱酸;
0.12mol/L的HB与0.10mol•L-1的NaOH溶液等体积混合,反应后剩余的酸的浓度为c(HB)=$\frac{0.12×V-0.1×V}{2V}$=0.01mol/L,溶液中c(H+)=0.01mol/l,所以HB完全电离,即NB为强酸;
A.由分析可知,HA是弱酸,HB是强酸,故A错误;
B.NaB强酸强酸碱盐,升高温度,B-、Na+的浓度不变,所以溶液②中$\frac{c({B}^{-})}{c(N{a}^{+})}$不变,故B错误;
C.溶液①中,恰好完全反应生成NaA,溶液的pH=8.7,显碱性,c(OH-)>c(H+),水解程度较小,所以c(A-)>c(OH-),则离子浓度的关系:c(Na+)>c(A-)>c(OH-)>c(H+),故C错误;
D.溶液②中c(H+)=0.01mol/l,c(B-)=0.12 mol•L-1×$\frac{1}{2}$=0.06mol/L,c(Na+)=0.1mol/L×$\frac{1}{2}$=0.05mol/L,所以c(Na+)+c(H+)+c(B-)=0.12 mol•L-1,故D正确.
故选D.
点评 本题考查了酸碱混合溶液定性判断和定量判断、弱电解质的电离、离子浓度大小的比较,题目难度中等,根据弱电解质的电离特点结合电荷守恒和物料守恒来分析解答.


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 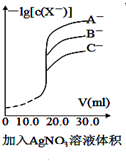 用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图可确定首先沉淀的是C- | |
| B. | 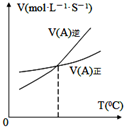 图表示反应中某反应物的正、逆反应速率随温度变化情况,由图可知该反应的正反应是吸热反应 | |
| C. | 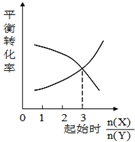 一定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X+3Y?Z | |
| D. | 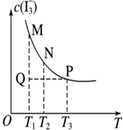 图表示溶液中反应:I2+I-?I3- 平衡c(I3-)随温度变化,反应速度V(正)M<V(逆)N |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 第Ⅱ步的离子方程式为Na++NH3+H2O+CO2→NaHCO3↓+NH4+ | |
| B. | 第Ⅲ步得到的晶体是Na2CO3•10H2O | |
| C. | A气体是CO2,B气体是NH3 | |
| D. | 第Ⅳ步操作的过程主要有溶解、蒸发、结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
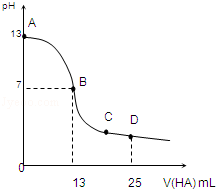 常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:
常温下,向25mL 0.1mol/L MOH溶液中逐滴加入0.2mol/L HA溶液,曲线如图所示(体积变化忽略不计).回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准NaOH溶液读数记录(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 | 2.0×10-48 | 2.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
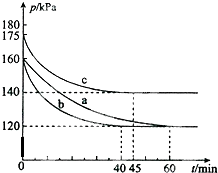 在10L的恒容密闭容器中,发生反应:PCl3(g)+Cl2(g)?PCl5(g)△H<0 若起始时PCl3(g)和Cl2(g)均为0.2mol,在不同条件下进行a、b、c三组实验,每一组实验都是在恒温恒容条件下进行,反应体系总压强随时间的变化如图所示.下列说法中正确的是( )
在10L的恒容密闭容器中,发生反应:PCl3(g)+Cl2(g)?PCl5(g)△H<0 若起始时PCl3(g)和Cl2(g)均为0.2mol,在不同条件下进行a、b、c三组实验,每一组实验都是在恒温恒容条件下进行,反应体系总压强随时间的变化如图所示.下列说法中正确的是( )| A. | 与实验a相比,实验b升高了温度,实验c加入了催化剂 | |
| B. | 从反应开始至刚达平衡时,实验b的化学反应速率ν(PCl5)=5×10-4mol/(L.min) | |
| C. | 实验c达平衡时,PCl3(g)的转化率为 60% | |
| D. | 在实验a条件下,该反应的平衡常数K=100 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 酸碱中和滴定是中学化学中重要的定量实验之一.某研究性学习小组准确进行了如下实验,称取1.00g不纯的苛性钠样品配成250ml溶液,取出10.00ml,用已知浓度为0.040mol•L-1的盐酸进行滴定(杂质不与盐酸反应).
酸碱中和滴定是中学化学中重要的定量实验之一.某研究性学习小组准确进行了如下实验,称取1.00g不纯的苛性钠样品配成250ml溶液,取出10.00ml,用已知浓度为0.040mol•L-1的盐酸进行滴定(杂质不与盐酸反应).| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗盐酸溶液的体积(mL) | 20.05 | 20.00 | 22.10 | 19.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 未知浓度盐酸用滴定管量取,该滴定管用蒸馏水洗涤后未用待测液润洗 | |
| B. | 装待测液的锥形瓶,洗涤后未干就盛入待测液 | |
| C. | 滴定结束后,用俯视法观察碱式滴定管刻度,其余操作正确 | |
| D. | 滴定结束后,发现碱式滴定管尖嘴处悬挂一滴碱液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
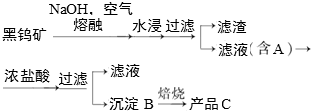
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com