
【题目】用未知浓度的盐酸滴定![]() NaOH溶液,下列操作使测定结果
NaOH溶液,下列操作使测定结果![]() 盐酸的浓度
盐酸的浓度![]() 偏低的是( )
偏低的是( )
A.酸式滴定管滴至终点后,俯视读数
B.滴定管滴定时,有一滴粘在锥形瓶壁上没用水冲洗
C.碱式滴定管用蒸馏水洗后,未用待测液润洗
D.酸式滴定管滴定完后发现尖嘴处有气泡
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】相同温度下,体积为2L的两个恒容容器中发生:![]() 均为气态物质
均为气态物质![]() 有下表所示实验数据:
有下表所示实验数据:
容器编号 | 起始时各物质的物质的量 | 达到平衡时体系能量的变化 | ||
|
|
| ||
① | 1 | 3 | 0 |
|
② | 0 | 0 | 2 |
|
③ |
|
|
|
|
下列有关说法正确的是
A.![]()
B.②中![]() 的转化率大于③中
的转化率大于③中![]() 的转化率
的转化率
C.容器①与③分别达到平衡时,平衡常数相同,且![]()
D.将容器①的反应条件换为恒温恒压中进行![]() 投料量不变
投料量不变![]() ,达到平衡时,气体平均摩尔质量较恒温恒容时减小了
,达到平衡时,气体平均摩尔质量较恒温恒容时减小了
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应是______________。在X极附近观察到的现象是______________________________。
②Y电极上的电极反应式是______________。检验该电极反应产物的方法是______________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是___________________,电极反应式是______________。
②Y电极的材料是___________________,电极反应式是______________。
(说明:杂质发生的电极反应不必写出)
③假若电路中有0.04摩尔电子通过时,阴极增重________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对含微量![]() 的某样品进行
的某样品进行![]() 化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用
化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用![]() 标准溶液滴定以求得
标准溶液滴定以求得![]() 的浓度。下列分析正确的是
的浓度。下列分析正确的是
已知:![]() 过量
过量![]()
方法一![]() 样品
样品![]()
![]()
![]() -
-![]()
![]()
![]()
![]()
![]()
方法二![]() 样品
样品![]()
![]() I2
I2![]()
![]()
A.方法二对样品所做处理操作简便,用作微量的测定更准确
B.当待测液由无色变为蓝色时即达到滴定终点
C.方法一与方法二测量出的样品浓度比为6:l
D.假设各步骤操作均得当,方法一所消耗![]() 标准溶液的体积是方法二的6倍
标准溶液的体积是方法二的6倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A、B、C、D、E、F、G有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C9H10O2,试回答下列有关问题。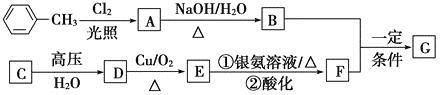
(1)G的结构简式为_______________________________。
(2)指出下列反应的反应类型:A转化为B:__________________,C转化为D:______________________。
(3)写出下列反应的化学方程式:
D生成E的化学方程式:________________________________。
B和F生成G的化学方程式:___________________________。
(4)符合下列条件的G的同分异构体有________种。
①苯环上有3个取代基,且有两个取代基相同;②能够与新制的银氨溶液反应产生光亮的银镜。其中共有四种不同化学环境氢原子的同分异构体的结构简式为_____________、____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
A.3 mol·L-1B.2 mol·L-1C.4 mol·L-1D.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知N2(g)+O2(g)![]() 2NO(g) ΔH=+181.5kJ·mol-1。某科研小组尝试利用固体表面催化工艺进行NO的分解,若用
2NO(g) ΔH=+181.5kJ·mol-1。某科研小组尝试利用固体表面催化工艺进行NO的分解,若用![]() 分别表示O2、N2、NO,则在固体催化剂表面分解NO的过程可用如图表示,下列说法正确的是( )
分别表示O2、N2、NO,则在固体催化剂表面分解NO的过程可用如图表示,下列说法正确的是( )

A.从吸附到解吸的过程中,能量状态最低的是C处
B.图示过程中,反应物断键吸收能量大于生成物形成新键释放的能量
C.该反应中NO分子浓度越大,分解速率越快
D.该反应中的固体催化剂起到反应载体的作用,未影响反应的速率,并且该反应的ΔH也不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次硫酸钠甲醛(xNaHSO2yHCHOzH2O)俗称吊白块,在印染、医药以及原子能工业中有广泛应用。它的组成可通过下列实验测定:①准确称取1.5400g样品,完全溶于水配成100mL溶液。②取25.00mL所配溶液经AHMT分光光度法测得甲醛物质的量浓度为0.10mol×L-1。③另取25.00mL所配溶液,加入过量碘完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体0.5825g。次硫酸氢钠和碘反应的方程式如下:xNaHSO2yHCHOzH2O+I2→NaHSO4+HI+HCHO+H2O(未配平)
(1)生成0.5825g白色固体时,需要消耗碘的质量为_____。
(2)若向吊白块溶液中加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物,写出该反应的离子方程式_____。
(3)通过计算确定次硫酸氢钠甲醛的组成______(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.12 g 金刚石中含有的共用电子对数为NA
B.1 mol AlCl3在熔融时离子总数为0.4NA
C.0.2 mol MnO2与足量浓盐酸反应转移的电子数小于 0.4NA
D.1 L 0.1 mol·Lˉ1 Na2CO3溶液中含有阴离子数大于 0.1 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com