
| A. | 二氧化硫气体通入过氧化钠:2SO2+2Na2O2═2Na2SO3+O2↑ | |
| B. | 金属铝投入NaOH溶液中:Al+2OH-═AlO${\;}_{2}^{-}$+H2↑ | |
| C. | 硫酸亚铁与酸性高锰酸钾反应:3Fe2++MnO${\;}_{4}^{+}$+4H+=3Fe3++MnO2↓+2H2O | |
| D. | 碳酸氢钠溶液与少量石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
分析 A.过氧化钠具有强氧化性,与二氧化硫反应生成硫酸钠,且该反应不是离子方程式;
B.2mol铝与氢氧化钠溶液反应生成3mol氢气,该反应不满足电子守恒;
C.反应中高锰酸根离子被还原生成锰离子;
D.石灰水的主要成分为氢氧化钙,氢氧化钙少量,反应生成碳酸钙沉淀、碳酸钠和水.
解答 解:A.二氧化硫气体通入过氧化钠,反应生成硫酸钠,且该反应无法书写离子方程式,故A错误;
B.金属铝投入NaOH溶液中,反应生成偏铝酸钠和氢气,正确的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故B错误;
C.硫酸亚铁与酸性高锰酸钾反应生成锰离子、铁离子和水,正确的离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,故C错误;
D.碳酸氢钠溶液与少量石灰水反应,离子方程式按照氢氧化钙的化学式书写,反应的离子方程式为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | Fe2O3 | SiO2 | NaOH | 过滤 |
| B | CO2 | CO | O2 | 点燃 |
| C | FeCl2溶液 | FeCl3 | Cu | 分液 |
| D | CH3CH2OH | H2O | Na | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定是单质 | B. | 一定是混合物 | ||
| C. | 可能是单质也可能是化合物 | D. | 可能单质是也可能是混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
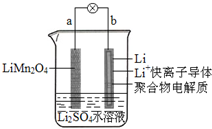 2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系.下列叙述错误的是( )
2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系.下列叙述错误的是( )| A. | a为电池的正极 | |
| B. | 电池放电反应为LiMn2O4=Li1-xMn2O4+xLi | |
| C. | 放电时,a极锂的化合价不发生变化 | |
| D. | 放电时,溶液中的Li+从b向a迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时,若阳极质量减少32g,则阴极转移的电子的数目为NA(注:粗铜含有Zn、Fe等杂质) | |
| B. | 含0.2mol H2SO4的浓硫酸与足量铜充分反应,生成SO2分子的数目少于0.1NA | |
| C. | 在标况下,22.4L SO3和22.4L C2H4原子个数比为2:3 | |
| D. | 将78g Na2O2与过量CO2反应,CO2转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 模拟对象 | 类推结论 | |
| A | 2HCl+Mg═MgCl2+H2↑ | H2SO4+2Na═Na2SO4+H2↑ |
| B | Cl2+2Fe2+═2 Fe3++2Cl- | I2+2Fe2+═2Fe3++2I- |
| C | Mg在O2中燃烧生成MgO | Na在O2中燃烧生成Na2O |
| D | Al在NaOH溶液中反应可产生H2 | Mg与NaOH溶液反应也可以产生H2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com