
【题目】分析下列反应回答相应问题.
①3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
未被还原的硝酸与参加反应的总硝酸的质量比为 .
②S+2KNO3+3C ![]() K2S+N2↑+3CO2↑ 还原剂是还原产物是
K2S+N2↑+3CO2↑ 还原剂是还原产物是
③3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移mol电子.
5NaCl+NaClO3+3H2O 反应中若消耗3molCl2共转移mol电子.
【答案】3:4;C;K2S、N2;5
【解析】解:①在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中,硝酸中N元素得电子被还原,作氧化剂,如果有8mol硝酸参加反应,则有2mol硝酸参加氧化还原反应,所以未被还原的硝酸与参加反应的总硝酸的质量比为6:8=3:4;
所以答案是:3:4;②S+2KNO3+3C═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,则氧化剂为S、KNO3 , 生成K2S、N2为还原产物,C元素的化合价升高,则还原剂为C,所以答案是:C;K2S、N2;③3molCl2完全反应电子转移3mol×2× ![]() (1﹣0)=5mol;
(1﹣0)=5mol;
所以答案是:5.


科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的判断正确的是( )
A. 60℃时,NaCl溶液的pH<7,则溶液呈酸性
B. 将pH=4的CH3COOH溶液加水稀释,溶液中所有离子的浓度均减小
C. 常温下,CH3COOH分子可能存在于pH>7的碱性溶液中
D. 相同温度下,1 mol·L-1氨水与0.5 mol·L-1氨水中c(OH-)之比是2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学方程式为3MnO2+6KOH+KClO3 ![]() 3K2MnO4+KCl+3H2O,下列说法中正确的( )
3K2MnO4+KCl+3H2O,下列说法中正确的( )
A.反应中MnO2是氧化剂
B.该反应属于复分解反应
C.KClO3在反应中失去电子
D.反应中每生成l mol K2MnO4 , 氧化剂得到2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
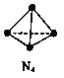
【题目】N4分子结构为正四面体(如图所示)。已知:断裂N4(g)中1 molN-N键吸收193kJ能量,形成N2(g)中1 mol N![]() N放出941 kJ能量。下列说法正确的是
N放出941 kJ能量。下列说法正确的是
A. N4(g)比N2(g)更稳定
B. N4(g)=2N2(g) △H=+724kJmol-1
C. 形成1 mol N4(g)中的化学键放出193 kJ的能量
D. lmolN2(g)完全转化为N4(g),体系的能量增加362kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列有机化合物的说法正确的是( )
A.溴乙烷和乙烷都是饱和烃
B.甲烷和乙烯都可以与氯气反应
C.高锰酸钾酸性溶液可以氧化苯和甲烷
D.乙烯可以与氢气发生加成反应,苯不能与氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) ΔH。
CH3OH(g) ΔH。
(1)能判断反应达到平衡状态的依据是__________(填字母序号)。
A.2 ν逆(H2) = ν 正(CO)
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
E.容器内CO、H2、CH3OH的浓度之比为1:2:1
F、CO、H2、CH3OH的速率之比为1:2:1
(2)CO在不同温度下的平衡转化率与压强的关系如图1,该反应△H_______0(填“>”或“<”)。

(3)一定温度下,将4a mol H2和2amol CO放入2L的密闭容器中,充分反应后测得CO的转化率为50%,则:
①该反应的平衡常数为_______________。
②若此时再向该容器中投入a mol CO、2amol H2和amol CH3OH,判断平衡移动的方向是_______________(“正向移动”“逆向移动”或“不移动”);
③在其他条件不变的情况下,将容器体积压缩到原来的![]() ,与原平衡相比,下列有关说法正确的是_____________(填字母)。
,与原平衡相比,下列有关说法正确的是_____________(填字母)。
A.H2的浓度减小; B.正反应速率加快,逆反应速率也加快;
C.甲醇的物质的量增加; D.重新平衡时, ![]() 增大;
增大;
(4)上图2表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A_________ C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A_________ C,由状态B到状态A,可采用_____________的方法(填“升温”或“降温”)。
(5)如图是一定的温度和压强下![]() 和
和![]() 反应生成1 mol
反应生成1 mol ![]() 过程中能量变化示意图,请写出工业合成氨的热化学方程式__________________
过程中能量变化示意图,请写出工业合成氨的热化学方程式__________________![]() H的数值用含字母
H的数值用含字母![]() 、Q
、Q![]() 的代数式表示)。
的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知空气-锌电池的电极反应为:锌片:Zn+20H--2e-=ZnO+H20 石墨:02+2H20+4e-=40H-根据此判断,锌片是
A.负极,并被氧化 B.负极,并被还原
C.正极,并被氧化 D.正极,并被还原、
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列实验事实:
①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;
②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液;
③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
A. 化合物KCrO2中Cr元素为+3价
B. 实验①证明Cr2O3是两性氧化物
C. 实验②证明H2O2既有氧化性又有还原性
D. 实验③证明氧化性: Cr2O72-> I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com