
烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫研究。
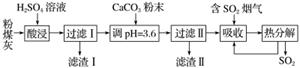
(1)酸浸时反应的化学方程式为________________________________;滤渣Ⅰ的主要成分为________________(填化学式)。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6-2x。滤渣Ⅱ的主要成分为________________________(填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是________________________________________(用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是________________________________;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将________(填“增大”“减小”或“不变”)。
答案 (1)Al2O3+3H2SO4===Al2(SO4)3+3H2O SiO2
(2)CaSO4 3CaCO3+2Al3++3SO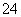 +3H2O===2Al(OH)3+3CaSO4+3CO2↑
+3H2O===2Al(OH)3+3CaSO4+3CO2↑
(3)溶液中的部分SO 被氧化成SO
被氧化成SO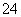 减小
减小
解析 (1)酸浸时能与H2SO4反应的是Al2O3,H2SO4与Al2O3反应生成盐和水,SiO2不和H2SO4反应,成为滤渣。
(2)CaCO3和溶液中的H2SO4反应生成CaSO4;如果pH偏高,一部分Al3+会转化为Al(OH)3沉淀,离子方程式为3CaCO3+2Al3++3SO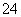 +3H2O===2Al(OH)3+3CaSO4+3CO2↑。
+3H2O===2Al(OH)3+3CaSO4+3CO2↑。
(3)热分解时,一部分亚硫酸盐被氧化为硫酸盐,不能分解成为SO2;SO2溶于水生成H2SO3,会中和溶液中的部分OH-,使溶液的pH减小。


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
关于共价键的说法,正确的是( )
A.一般来说σ键键能小于π键键能
B.原子形成共价键的数目等于基态原子的未成对电子数
C.相同原子间的双键键能是单键键能的两倍
D.所有不同原子间的键至少具有弱极性
查看答案和解析>>
科目:高中化学 来源: 题型:
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH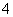 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO 、SO
、SO 、CO
、CO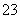 ,已知:
,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是____________;所含阴离子相同的两种盐的化学式是__________________。
(2)D的化学式为__________________,D溶液显碱性的原因是________________________________________________________________________(用离子方程式表示)。
(3)A和C的溶液反应的离子方程式是________________________________________________________________________;
E和氨水反应的离子方程式是________________________________________________________________________。
(4)若要检验B中所含的阳离子,正确的实验方法是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色溶液中:ClO-、MnO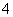 、Al3+、K+
、Al3+、K+
B.1.0 mol·L-1的NaAlO2溶液中:Cl-、HCO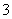 、K+、Ca2+
、K+、Ca2+
C.在强碱性环境中:AlO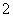 、SiO
、SiO 、Na+、K+
、Na+、K+
D.能使甲基橙显红色的溶液中:NH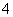 、AlO
、AlO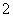 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
向30 mL 1 mol·L-1的AlCl3溶液中逐渐加入浓度为4 mol·L-1的NaOH溶液,若产生0.78 g白色沉淀,则加入的NaOH溶液的体积可能为( )
A.3 mL B.7.5 mL
C.15 mL D.17.5 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2Na[Al(OH)4]+CO2—→2Al(OH)3↓+Na2CO3+H2O。向含2 mol NaOH、1 mol Ba(OH)2、2 mol Na[Al(OH)4]的混合溶液中慢慢通入CO2,则通入CO2的量和生成沉淀的量的关系正确的是( )
| 选项 | A | B | C | D |
| n(CO2)(mol) | 2 | 3 | 4 | 6 |
| n(沉淀)(mol) | 1 | 2 | 3 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两烧杯中分别装有相同体积、相同pH的氨水和NaOH溶液,各加入10 mL 0.1 mol·L-1 AlCl3溶液,两烧杯中都有沉淀生成。下列判断正确的是( )
A.甲中沉淀一定比乙中的多
B.甲中沉淀可能比乙中的多
C.甲中沉淀一定比乙中的少
D.甲中和乙中的沉淀一定一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程与配合物的形成无关的是( )
A.除去Fe粉中的SiO2可用强碱溶液
B.向一定量的AgNO3溶液中加入氨水至沉淀消失
C.向含Fe3+的溶液中加入KSCN溶液
D.向一定量的CuSO4溶液中加入氨水至沉淀消失
查看答案和解析>>
科目:高中化学 来源: 题型:
通常情况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是( )
A.分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B.分子中的所有原子均达到8电子稳定结构
C.NCl3分子是非极性分子
D.NBr3比NCl3易挥发
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com