
 bZ(g)
bZ(g)| A.a=1,b=1 | B.a=2,b=1 |
| C.a=2,b=2 | D.a=3,b=3 |
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源:不详 题型:单选题
 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )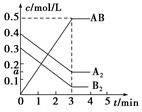
| A.图中a点的值为0.15 |
| B.该反应的平衡常数K=0.03 |
| C.温度升高,平衡常数K值减小 |
| D.平衡时A2的转化率为62.5% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如下图,下列有关说法一定正确的是( )
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如下图,下列有关说法一定正确的是( )
| A.上述反应的ΔH>0 |
| B.压强p1>p2>p3>p4 |
| C.1 100 ℃该反应的平衡常数为64 |
| D.压强为p4时,在Y点:v(正)<v(逆) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
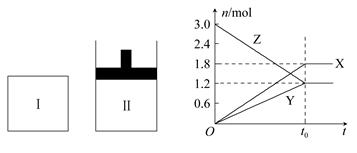
A.该反应的化学方程式:3X+2Y 3Z 3Z |
| B.若两容器中均达到平衡后,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所用时间小于t0 |
| C.若两容器中均达到平衡后,两容器中Z的物质的量分数相同,则Y为固态或液态 |
| D.达平衡后,若对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是 ( )
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是 ( )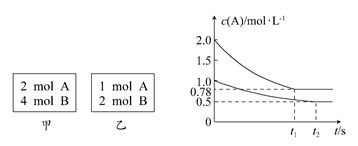
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92| A.常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2) |
| B.常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C.常温下,NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 |
| D.以上说法都不正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在平衡常数表达式中,反应物浓度用起始浓度表示,生成物浓度用平衡浓度表示 |
| B.化学平衡常数较大的可逆反应,所有反应物的转化率一定大 |
| C.可以用化学平衡常数来定量描述化学反应的限度 |
| D.平衡常数的大小与温度、浓度、压强、催化剂有关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g) ΔH<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是 ( )
2C(g) ΔH<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是 ( )| | X | Y |
| A | 再加入A | B的转化率 |
| B | 加入催化剂 | A的体积分数 |
| C | 充入氦气 | A的转化率 |
| D | 升高温度 | C的体积分数 |
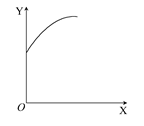
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 TaI4(g)+S2(g) ΔH>0(I)
TaI4(g)+S2(g) ΔH>0(I)
 HSO3-+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
HSO3-+H+的电离常数Ka=1×10-2mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kh=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中 将________(填“增大”“减小”或“不变”)。
将________(填“增大”“减小”或“不变”)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com