
【题目】A、B、C、D是四种短周期元素,E是过渡金属元素。A、B、C同周期,C、D同主族,A的原子结构示意图为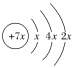 ,B的核外电子排布式为1s22s22p63s1,C的最外层有三个未成对电子,E的价电子排布式为3d64s2。试回答下列问题:
,B的核外电子排布式为1s22s22p63s1,C的最外层有三个未成对电子,E的价电子排布式为3d64s2。试回答下列问题:
(1)写出下列元素的名称:A__________,C________。
(2)E元素原子的未成对电子数是________,E元素在周期表中位于第________周期______族;已知元素周期表可按电子排布分为s区、p区、d区等,则E元素在______区。
(3)画出D的核外电子排布图:_________。
【答案】硅 磷 4 四 Ⅷ d ![]()
【解析】
A、B、C、D是四种短周期元素, K层最多排列2个电子,所以x=2,A的原子结构示意图为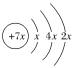 ,则A原子核内有14个质子,A为Si元素;A、B、C同一周期,B核外电子排布式为1s22s22p63s1,则B是Na元素,C的最外层有三个未成对电子,则C为P元素;C、D同主族,且D属于短周期元素,则D为N元素;E是过渡元素,E的外围电子排布式为3d64s2,E的核外电子总数为:2+8+8+6+2=26,则E为Fe元素,据此解答。
,则A原子核内有14个质子,A为Si元素;A、B、C同一周期,B核外电子排布式为1s22s22p63s1,则B是Na元素,C的最外层有三个未成对电子,则C为P元素;C、D同主族,且D属于短周期元素,则D为N元素;E是过渡元素,E的外围电子排布式为3d64s2,E的核外电子总数为:2+8+8+6+2=26,则E为Fe元素,据此解答。
根据上述分析可知A是Si元素;B是Na元素;C是P元素;D是N元素;E是Fe元素。
(1) A是Si元素,元素名称为硅;C是P元素,元素名称为磷;
(2)E为Fe元素,外围电子排布式是3d64s2,d能级轨道数目为5,同一轨道最多能容纳2个自旋方向相反的电子,原子核外各个能级上电子总是尽可能成单排列,而且自旋方向相同,这样能量最低,所以Fe元素原子的未成对电子数是4个;Fe原子序数是26,Fe在元素周期表中位于第四周期第VIII族,属于d区元素;
(3)D为N元素,N原子核外电子排布式为1s22s22p3,电子排布图为![]() 。
。


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的立体构型,有时也能用来推测键角大小,下列判断正确的是( )
A.SO2、CS2、HI都是直线形分子B.BF3键角为120°,H2S键角大于120°
C.CH2O、BF3、SO3都是平面三角形分子D.PCl3、NH3、PCl5都是三角锥形分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。
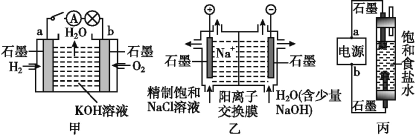
(1)甲装置中,a电极的反应式为_______________________________________。
(2)乙装置中,阴极区产物为________和_______。
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为_______(填“正”或“负”)极,该装置内,发生的电解方程式为___________________________________、生成消毒液的方程式为________________________________________________________。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为___________(不考虑气体的溶解)。
(5)某工厂采用电解法处理含Cr2O72-的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,Cr2O72-被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图:
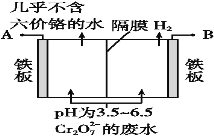
①写出电解时阳极的电极反应式:______________________________________。
②写出Cr2O72-被还原为Cr3+的离子方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图中装置进行实验,实验一段时间后,现象与预测不一致的是
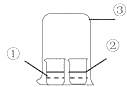
①中物质 | ②中物质 | 实验预测 | |
A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳定物质,如图:

![]() 是六种有机化合物,它们之间的关系如图:
是六种有机化合物,它们之间的关系如图:

请根据要求回答。
![]() 中含有的官能团是 ______
中含有的官能团是 ______ ![]() 填名称
填名称![]() 。
。
![]() 反应
反应![]() 的化学方程式为 ______ ,此反应的类型是 ______ 。
的化学方程式为 ______ ,此反应的类型是 ______ 。
![]() 已知B的相对分子质量为162,其完全燃烧的产物中
已知B的相对分子质量为162,其完全燃烧的产物中![]() :
:![]() :1,则B的分子式为 ______ 。
:1,则B的分子式为 ______ 。
![]() 是高分子光阻剂生产中的主要原料。F具有如下特点:
是高分子光阻剂生产中的主要原料。F具有如下特点:![]() 能跟FeCl3溶液发生显色反应;
能跟FeCl3溶液发生显色反应;![]() 能发生加聚反应;
能发生加聚反应;![]() 苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 ______ 。
苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 ______ 。
![]() 的结构简式是 ______ 。
的结构简式是 ______ 。
![]() 的同分异构体中含有苯环且能发生银镜反应的共有 ______ 种,其中核磁共振氢谱有4种不同化学环境的氢的是 ______
的同分异构体中含有苯环且能发生银镜反应的共有 ______ 种,其中核磁共振氢谱有4种不同化学环境的氢的是 ______ ![]() 写结构简式
写结构简式![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp(25℃)如表所示:
AgCl | AgI | Ag2S | |
Ksp | 1.8×1010 | 8.3×1017 | 6.3×1050 |
下列叙述错误的是
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀可以转化为溶解度更小的沉淀
C.AgCl固体分别在等浓度的氯化钾和氯化钙溶液中的溶解度是相同的
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各实验装置图的叙述中正确的是
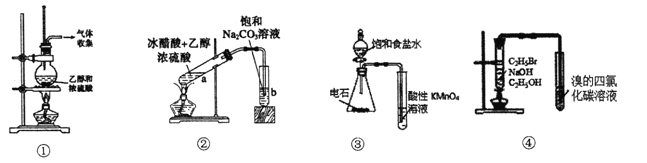
A. 装置①:实验室制取乙烯
B. 装置②:实验室制取乙酸乙酯
C. 装置③:验证乙炔的还原性
D. 装置④:验证溴乙烷发生消去反应可生成烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)
(1)向一定物质的量浓度的Cu(NO3)2 和Mn(NO3)2 溶液中加入Na2CO3 溶液,所得沉淀经高温灼烧,可制得CuMn2O4,NO3﹣的空间构型是______________________(用文字描述).
(2)在铜锰氧化物的催化下,CO 被氧化为CO2,HCHO 被氧化为CO2 和H2O.
①根据等电子体原理,CO 分子的结构式为____________.
②H2O 分子中O 原子轨道的杂化类型为____________.
③1mol CO2 中含有的σ键数目为__________________.
(3)H2SeO3的K1和K2分别为2.7×10﹣3和2.5×10﹣8,H2SeO4第一步几乎完全电离,K2为1.2×10﹣2,请根据结构与性质的关系解释:H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:_______________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向碳酸溶液中滴加NaOH溶液,测得碳酸中含碳微粒的物质的量分数随pH变化如下图所示,下列说法不正确的是

A.人体血液的pH=7.35~7.45,其中含碳微粒以HCO3-、H2CO3为主
B.除去NaCl溶液中Na2CO3的方法是向其中加入盐酸至pH=7
C.pH=10的溶液中c(H+)+c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)
D.将CO2通入NaOH溶液制取Na2CO3,应大约控制pH>12.5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com