
 ��1��ij����С����Ƶ�ʵ������ȡ����������װ����ͼ��ʾ��A��ʢ��Ũ���ᣬB��ʢ���Ҵ������ᣬD��ʢ�б���̼������Һ��
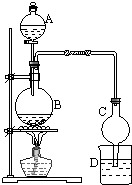
��1��ij����С����Ƶ�ʵ������ȡ����������װ����ͼ��ʾ��A��ʢ��Ũ���ᣬB��ʢ���Ҵ������ᣬD��ʢ�б���̼������Һ������ ��1�����Ҵ���������ȡ����������Ϊ������Ӧ������ȡ����Ӧ��
�ڴ���H���������ǻ�����������������ˮ��
���Ҵ�������������ˮ�����θ����C�е����νṹ�ɷ�ֹҺ�嵹����
�ܱ���̼������Һ�������Ҵ�����ȥ���ᣬ���������������ܽ�ȣ�
�ݷ�Ӧ��̼������Һ�����������ֲ㣬�������������ܶȱ�ˮ���ܶ�С��
��2��A���ƾ���ˮ���ܣ���������ȡ����
B��Һ��ʯ���������ͺ�ʯ������Ҫ�ɷ־�Ϊ�������ʣ�
C��������Ӧ��֪����ˮ�����������ǣ�����Ҫ��ˮ��������Ƿ�ʣ�ࣻ
D��������140�淢�����Ӽ���ˮ�������ѣ�
E���������м���NaOH��Һ�����ȣ�����ˮ�������Ҵ���NaBr����ȴ����ϡ��������Һ�����ԣ��ټ����������������ӣ�
��� �⣺���Ҵ���������ȡ���������ķ�Ӧ������ȡ����Ӧ���ʴ�Ϊ��ȡ����Ӧ��
������18O����Ҵ��е���ԭ�ӣ���CH3CH218OH�����ᷴӦ�Ļ�ѧ����ʽ��CH3COOH+C2H518OH$?_{��}^{ŨH_{2}SO_{4}}$ CH3CO18OC2H5+H2O��
�ʴ�Ϊ��CH3COOH+C2H518OH$?_{��}^{ŨH_{2}SO_{4}}$ CH3CO18OC2H5+H2O��
�����θ����C�������Ƿ�ֹ�������ʴ�Ϊ����ֹ������
��D��ѡ�ñ���̼������Һ��ԭ�������������뱥��Na2CO3��Һ�����ܡ����ܶ��нϴ���죬�����ڷֲ㣬����Na2CO3��Һ���������ջӷ�������������Ҵ���
�ʴ�Ϊ�����������뱥��Na2CO3��Һ�����ܡ����ܶ��нϴ���죬�����ڷֲ㣬����Na2CO3��Һ���������ջӷ�������������Ҵ���
�ݷ�Ӧ������D�е�������Һ��ֲ㡢�ϲ�Ϊ��ɫ��״Һ�壬�ʴ�Ϊ��Һ��ֲ㡢�ϲ�Ϊ��ɫ��״Һ�壻
��2��A���ƾ���ˮ���ܣ���������ȡ����Ӧѡ�������Ȼ�̼��ȡ����A����
B��Һ��ʯ���������ͺ�ʯ������Ҫ�ɷ־�Ϊ�������ʣ�����̼�⻯�����B��ȷ��
C��������Ӧ��֪����ˮ�����������ǣ�����Ҫ��ˮ��������Ƿ�ʣ�࣬���ʵ�鲻��֤������ˮ�⣬��C����
D��������140�淢�����Ӽ���ˮ�������ѣ�Ӧ���ȵ�170�淢����ȥ��Ӧ������ϩ����D����
E���������м���NaOH��Һ�����ȣ�����ˮ�������Ҵ���NaBr����ȴ����ϡ��������Һ�����ԣ�����AgNO3��Һ�۲��Ƿ��е���ɫ�������ɿɼ��������ӣ���E��ȷ��
�ʴ�Ϊ��B E��
���� ���⿼���л�����Ʊ�ʵ�鼰��ѧʵ�鷽�������ۣ�Ϊ��Ƶ���㣬����ʵ��װ�õ����á�ʵ�鼼�ܡ��л���Ľṹ������Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע���л������ʵ�Ӧ�ã���Ŀ�ѶȲ���


 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д� ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | 0.1mol/L H2C2O4 ��Һ�����/mL | 0.01mol/L ���� KMnO4 �����/mL | ����ˮ�����/mL | �¶�/�� |
| �� | 2 | 4 | 2 | 25 |
| �� | 3 | |||
| �� | 50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
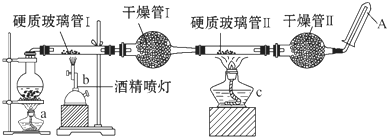 �ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe����ˮ����������Ӧ��Ӧ������װ�ã���̽����Ӧ�IJ��ֲ����Ӳ�ʲ����ܢ��з��뻹ԭ���ۺ�ʯ���Ļ���Ӳ�ʲ����ܢ��м���CuO������ܢ���ʢװ����������ˮ����ͭ��ʯ���Ļ����
�ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe����ˮ����������Ӧ��Ӧ������װ�ã���̽����Ӧ�IJ��ֲ����Ӳ�ʲ����ܢ��з��뻹ԭ���ۺ�ʯ���Ļ���Ӳ�ʲ����ܢ��м���CuO������ܢ���ʢװ����������ˮ����ͭ��ʯ���Ļ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 FeCl3•6H2O����
FeCl3•6H2O�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
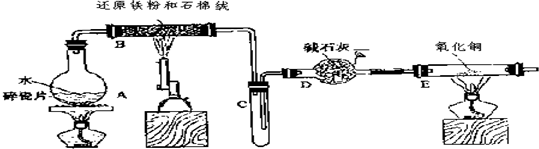
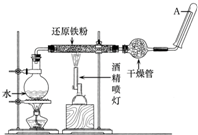 �ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe��ˮ�����ɷ�����Ӧ��Ӧ������װ�ã���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ���Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ����¡�Fe��ˮ������Ӧ��ʵ�顱��
�ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe��ˮ�����ɷ�����Ӧ��Ӧ������װ�ã���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ���Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ����¡�Fe��ˮ������Ӧ��ʵ�顱���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
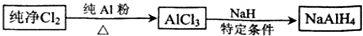
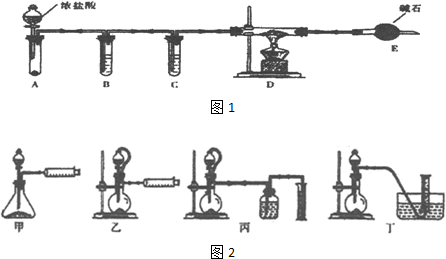
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
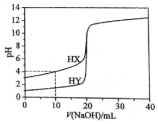 �����£���Ũ��Ϊ0.1000mol•L-1��NaOH��Һ�ֱ���μ��뵽20.00mL 0.1000mol•L-1��HX��HY��Һ�У�pH��NaOH��Һ����ı仯��ͼ������˵����ȷ��������
�����£���Ũ��Ϊ0.1000mol•L-1��NaOH��Һ�ֱ���μ��뵽20.00mL 0.1000mol•L-1��HX��HY��Һ�У�pH��NaOH��Һ����ı仯��ͼ������˵����ȷ��������| A�� | V��NaOH��=10.00 mLʱ��c��X-����c��Na+����c��H+����c��OH-�� | |
| B�� | V��NaOH��=20.00 mLʱ��������Һ�У�c��X-����c��Y-�� | |
| C�� | V��NaOH��=20.00 mLʱ��c��Na+����c��X-����c��OH-����c��H+�� | |
| D�� | pH=7ʱ��������Һ�У�c��X-��=c��Y-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com