
【题目】如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( )

A.X是NH3,Y是水
B.X是SO2,Y是NaOH浓溶液
C.X是CO2,Y是稀硫酸
D.X是HCl,Y是NaNO3稀溶液
【答案】C
【解析】
试题分析:挤压胶头滴管,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起,说明锥形瓶内压强减小,X可能溶于Y或与Y发生反应.
解:A、NH3极易溶于水,NH3溶于水时,锥形瓶中的压强减小,能够导致小气球a鼓起,气体X和液体Y可能是NH3和水,故A正确;
B、SO2能够与NaOH浓溶液反应,SO2被吸收,锥形瓶中的压强减小,能够导致小气球a鼓起,气体X和液体Y可能是SO2和NaOH浓溶液,故B正确;
C、CO2与稀硫酸不反应,难溶于稀硫酸溶液,压强基本不变,小气球不能鼓起,气体X和液体Y不可能是CO2和稀硫酸,故C错误;
D、氯化氢不与NaNO3反应,但氯化氢极易溶于水,氯化氢溶于水时,锥形瓶中的压强减小,能够导致小气球a鼓起,气体X和液体Y可能是氯化氢和NaNO3稀溶液,故D正确;
故选C.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子既能与镁粉反应,又能大量共存,且其溶液为无色溶液的是
A.Ca2+、Cl-、MnO4-、Na+B.K+、Cl-、SO42-、H+
C.OH-、Na+、Al3+、I-D.H+、Cl-、Ba2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸二甲酯(CO(OCH3))是一种无毒、环保性能优异、用途广泛的化工原料。在催化剂作用下,可由甲醇和CO2直接合成:CO2+2CH3OH→CO(OCH3)2+H2O。某研究小组在某温度下,在0.1L恒容密闭容器中投入2.5molCH3OH(g)、适量CO2和6×10-5mol催化剂,研究反应时间对甲醇转化数(TON)的影响,其变化曲线如图所示。计算公式为:TON=转化的甲醇的物质的量/催化剂的物质的量。下列说法不正确的是
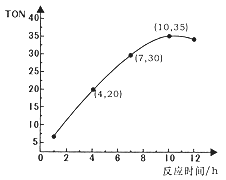
A. 在该温度下,最佳反应时间是10h
B. 4~10h内碳酸二甲酯的平均反应速率是7.5×10-4mol·L-1·h-1
C. 向反应体系中添加催化剂,一定能提高反应的TON
D. 该合成方法可以利用廉价的甲醇把影响环境的温室气体CO2转化为资源,在资源循环利用和环境保护方面具有重要意义
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:元素X、Y的核电荷数分别是a和b,它们的离子Xm+和Yn-的核外电子排布相同,则下列关系式中正确的是( )
A.a-m=b+nB.a+m=b-n
C.a-n=b+mD.a+n=b-m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了防止氮氧化物对空气的污染,人们采取了很多措施。
(1)如用CH4催化还原NO2可以消除氮氧化物的污染,发生的反应如下: CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1。
N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1。
①下列有关说法正确的是_________。
A.在容器中充入1mol CH4和2 mol NO2,当体系中n(CH4)/n(NO2)比值不随时间变化时,反应达到平衡状态
B.恒温恒容时,当混合气体的密度不随时间变化时,该反应达到平衡状态
C.体系达到平衡后,升高温度,体系中的混合气体的平均相对分子质量增大
D.恒温恒压时,充入CH4有利于提高氮氧化物的转化率
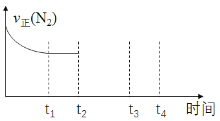
②在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态。请在右图中补充画出从t2到t4时刻v正(N2) 随时间的变化曲线:____________
(2)现有的汽车尾气处理的原理是:NO(g)+2CO(g)![]() N2(g) +2CO2(g),通常使含适当比例的NO、CO尾气通过装有高效催化剂的处理装置。请根据以下相关数据,分析仅使用催化剂能否有效消除NO、CO尾气污染___________。
N2(g) +2CO2(g),通常使含适当比例的NO、CO尾气通过装有高效催化剂的处理装置。请根据以下相关数据,分析仅使用催化剂能否有效消除NO、CO尾气污染___________。
反应 | 25℃时的平衡常数 | 焓变 |
反应I:2NO(g) | K1=1×1030 | △H=-180.5kJ/mol |
反应II:2CO2 (g) | K2=4×10-92 | △H= +566.0kJ/mol |
(3)用NH3催化还原NOx也可以消除氮氧化物的污染,其反应原理为:NO(g) +NO2(g)+2NH3(g)![]() 2N2(g) + 3H2O(g)。一定温度下,在某恒定压强为P的密闭容器中充入一定量的NO、NO2和NH3,达到平衡状态后,容器中含n(NO)=a mol,n(NO2)=2a mol,n(NH3)=2a mol,n(N2)=2b mol,且N2(g)的体积分数为1/3,请计算此时的平衡常数Kp=________________。(用只含P的式子表示,且化至最简式)。(备注:对于有气体参加的反应,可用某组分的平衡分压代替物质的量浓度计算平衡常数,记作KP。如p(NO2)为NO2的平衡分压,p(NO2)=x(NO2)p,p为平衡总压,x(NO2)为平衡体系中NO2的物质的量分数。)
2N2(g) + 3H2O(g)。一定温度下,在某恒定压强为P的密闭容器中充入一定量的NO、NO2和NH3,达到平衡状态后,容器中含n(NO)=a mol,n(NO2)=2a mol,n(NH3)=2a mol,n(N2)=2b mol,且N2(g)的体积分数为1/3,请计算此时的平衡常数Kp=________________。(用只含P的式子表示,且化至最简式)。(备注:对于有气体参加的反应,可用某组分的平衡分压代替物质的量浓度计算平衡常数,记作KP。如p(NO2)为NO2的平衡分压,p(NO2)=x(NO2)p,p为平衡总压,x(NO2)为平衡体系中NO2的物质的量分数。)
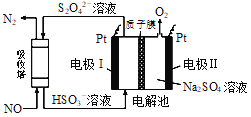
(4)用间接电化学法对大气污染物NO进行无害化处理,其原理示意如图(质子膜允许H+和H2O通过),电极I发生的电极反应为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L的密闭容器中发生反应后各物质的物质的量随时间变化的曲线如图所示。

回答下列问题:
(1)该反应的反应物和生成物分别是_______________,反应方程式为_______。
(2)0~10 s的平均反应速率v(H2)= ________v(HI)=____________________。
(3)根据上述反应速率数值,分析用不同物质表示同一化学反应在同一时间内,化学反应速率值是否必须相同?_________________________________________。
(4)能否用I2(s)表达该反应的反应速率,为什么?__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.化石能源物质内部蕴含着大量的能量
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在一定条件下转化为热能、电能,为人类所利用
D.吸热反应没有利用价值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com