
关于电离能的下列理解中错误的是( )
A.电离能可以表示原子或离子失去电子的难易程度
B.某原子的电离能越小,表示在气态时该原子越容易失去电子
C.第二电离能是气态+1价阳离子失去一个电子所需要的最小能量
D.电离能跟金属活动性顺序是对应的
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)因漂白粉在空气中不稳定,故可用于漂白纸张(×)
(2014·江苏,4C)
(2)用惰性电极电解熔融NaCl:2Cl-+2H2O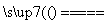 Cl2↑+H2↑+2OH-(×)
Cl2↑+H2↑+2OH-(×)
(2010·江苏,3A)
查看答案和解析>>
科目:高中化学 来源: 题型:
在1.0 L密闭容器中放入0.10 mol A(g),在一定温度进行如下反应:
A(g)B(g)+C(g) ΔH=+85.1 kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100 kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为__________。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为__________。平衡时A的转化率为__________,列式并计算反应的平衡常数K________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n(总)=________ mol,n(A)=________ mol。
②下表为反应物A浓度与反应时间的数据,计算:a=________。
| 反应时间t/h | 0 | 4 | 8 | 16 |
| c(A)/(mol·L-1) | 0.10 | a | 0.026 | 0.006 5 |
分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是________________,由此规律推出反应在12 h时反应物的浓度c(A)为__________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A(g)+B(g)C(g)+D(g),反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830 ℃时,向一个2 L的密闭容器中充入0.2 mol的A和0.8 mol的B,反应初始4 s内A的平均反应速率v(A)=0.005 mol·L-1·s-1。下列说法中正确的是( )
A.4 s时c(B)为0.76 mol·L-1
B.830 ℃达平衡时,A的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1 200 ℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为0.4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.同族元素,随着电子层数的增加,I1逐渐增大
B.同周期元素,随着核电荷数的增加,I1逐渐增大
C.通常情况下,电离能I1<I2<I3
D.电离能越小,元素的金属性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素M的逐级电离能(kJ·mol-1)分别为580,1 820,2 750,11 600。该元素氧化物的化学式最可能是( )
A.MO B.MO2
C.MO3 D.M2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com