
| A. | [Na+]>[A-]>[H+]>[OH-] | B. | [Na+]>[OH-]>[A-]>[H+] | C. | [Na+]+[OH-]=[A-]+[H+] | D. | [Na+]+[H+]=[A-]+[OH-] |
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:H2SeO4>Cl2H2SeO3>H2SO4 | |
| B. | 在SO2与亚硒酸的反应中,1mol H2SeO3参加反应转移4mol e- | |
| C. | 析出1mol硒需要消耗标准状况下22.4 L SO2 | |
| D. | 亚硒酸既有氧化性,又有还原性 |
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:选择题
钢铁生锈过程发生如下反应:
①2Fe+O2+2H2O=2Fe(OH)2;
②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
③2Fe(OH)3=Fe2O3+3H2O。
下列 说法正确的是
说法正确的是
A.反应①、②中电子转移数目相等
B.反应①中氧化剂是氧气和水
C.与铜质水龙头连接处的钢质水管不易发生腐蚀
D.钢铁在潮湿的空气中不能发生电化学腐蚀
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
用二氧化氯(ClO2)新型净水剂替代传统的净水剂Cl2,对淡水进行消毒是城市饮用水处理的新技术,其中纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物与NaClO3反应生成ClO2。则消耗1mol最终产物转移电子的物质的量为
A.6mol B.20mol C.12 mol D.24mol
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②③④⑤ | C. | ①③⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
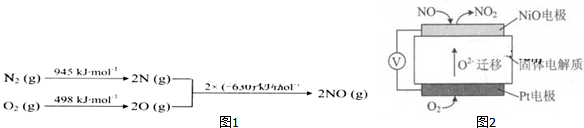
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有化学键破坏的变化一定属于化学变化 | |
| B. | 发生了颜色变化的一定是化学变化 | |
| C. | 有气泡产生或沉淀析出的变化一定是化学变化 | |
| D. | 燃烧一定是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
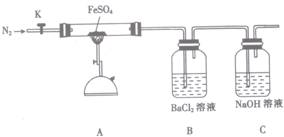
| 操作步骤 | 实验现象 | 用化学方程式解释原因 |
| 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | 洗气瓶B中①有白色沉淀生成 | ②SO3+H2O+BaCl2=BaSO4↓+2HCl |
| A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到③有红棕色固体物质生成 | ④2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑ |
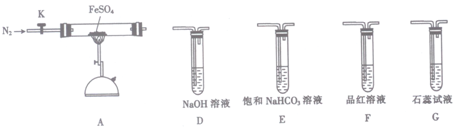
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com