
��14�֣������������ƣ�Na2S2O4���׳Ʊ��շۣ���һ��ǿ��ԭ�����㷺���ڷ�֯��ҵ��
���Ʊ��������£�
�ٰѼ��ᣨHCOOH����������NaOH��Һ��ϣ�
����Na2SO3�����ij�ᷴӦ�Ʊ�SO2���壻
����һ���¶��£���������SO2����ͨ��ٵ���Һ�У����б��շ����ɣ�ͬʱ����һ�����塣
��1��д��NaOH�ĵ���ʽ
��2���Ʊ�SO2ʱ��ѡ�õ��ᣬ����Ϊ����������ѡ�õ���
A��Ũ���� B����������Ϊ70%��H2SO4
C��ϡ���� D����������Ϊ10%��ϡ����
��3���Ʊ����շ۵Ļ�ѧ����ʽ�ɱ�ʾΪ
��4�����շۿ������ڳ�ȥ��ˮ�е��ظ�������ӣ�Cr2O72-��ת��ΪCr3+��������Ŀǰ��ȥ���Է�ˮ�и����ӵ���Ч����֮һ����ÿ����0��1mol���շۣ������Ͽ��Գ�ȥCr2O72-�����ʵ���Ϊ mol��
��5�����շ۲��ȶ������ֽ����ɼס� �ҡ� �����ֻ���������ס����������ʷֱ������Һ���ڼ���Һ�м���ϡ���ᣬ���е���ɫ���������������������Һ�м���BaCl2��Һ��ϡ���ᣬ����������������ް�ɫ�������ڼ���Һ�м���ϡ�������������Ӧ�����ӷ���ʽΪ ���շ۷ֽ�Ļ�ѧ����ʽΪ
��6�����շ��ڿ������������������������������䷽��ʽΪ��
��2Na2S2O4+O2+H2O=4NaHSO3 �� ��2Na2S2O4+O2+H2O=4NaHSO3+NaHSO4
�����ʵ��֤������ʱ�������Ǣڵķ�Ӧ��
(1)  (2) B
(2) B
(3) NaOH+HCOONa+2SO2=Na2S2O4+CO2+H2O��дHCOOH����ƽû���⣬Ҳ���֣�
(4) 0��1
(5) S2O32-+2H+=SO2+S��+H2O 2 Na2S2O4 = Na2S2O3+Na2SO3+SO2
(6) ȡ������������ˮ��,����BaCl2��Һ���а�ɫ������������֤���Ǣ�
����ȡ������������ˮ�У����ŵ��̼�����ζ����֤���Ǣڣ�
��������
�����������1��NaOH�ĵ���ʽΪ ����2���Ʊ�SO2ʱ��ѡ�õ��ᣬA����Ũ���� �ƵõĶ��������к����Ȼ��⣬����B������������Ϊ70%��H2SO4�ƶ������ɼ��ٶ���������ܽ���ʧ�������ڶ��������ݳ�����ȷ��C��ϡ�����ܽ�������������������D������������Ϊ10%��ϡ���ᣬ���������ܽ���ʧ������ѡB����3����������֪���Ʊ����շ۵�ԭ��Ϊ�����������ƺ��������Ʒ�Ӧ���ɱ��շۣ���ѧ����ʽ�ɱ�ʾΪNaOH+HCOONa+2SO2=Na2S2O4+CO2+H2O����4�����շ۳�ȥ���Է�ˮ�е��ظ�������ӣ�Cr2O72-��ת��ΪCr3+���ķ�Ӧ����ʽΪ��6H++Cr2O72-+ S2O42��== 2Cr3++ 2SO42��+3 H2O����ÿ����0.1mol���շۣ������Ͽ��Գ�ȥCr2O72-�����ʵ���Ϊ0.1 mol����5����������֪������ҺΪNa2S2O3��Һ�������м���ϡ��������������ơ��������������ˮ��������Ӧ�����ӷ���ʽΪS2O32-+2H+=SO2+S��+H2O�����շ۷ֽ�������������ơ��������ƺͶ�������ѧ����ʽΪ2 Na2S2O4 = Na2S2O3+Na2SO3+SO2����6�����շ��ڿ�������������������������������������Ӧ�ڣ�2Na2S2O4+O2+H2O=4NaHSO3+NaHSO4������ΪNaHSO3��NaHSO4�Ļ���Ҫ֤������ʱ�������Ǣڵķ�Ӧ���ɼ�������������ɣ�ʵ�鷽��Ϊ��ȡ������������ˮ�У�����BaCl2��Һ���а�ɫ������������֤���Ǣڣ�Ҳ������H++HSO3��==H2O+SO2�����ʵ�飬ʵ�鷽��Ϊ��ȡ������������ˮ�У����ŵ��̼�����ζ����֤���Ǣڡ�
����2���Ʊ�SO2ʱ��ѡ�õ��ᣬA����Ũ���� �ƵõĶ��������к����Ȼ��⣬����B������������Ϊ70%��H2SO4�ƶ������ɼ��ٶ���������ܽ���ʧ�������ڶ��������ݳ�����ȷ��C��ϡ�����ܽ�������������������D������������Ϊ10%��ϡ���ᣬ���������ܽ���ʧ������ѡB����3����������֪���Ʊ����շ۵�ԭ��Ϊ�����������ƺ��������Ʒ�Ӧ���ɱ��շۣ���ѧ����ʽ�ɱ�ʾΪNaOH+HCOONa+2SO2=Na2S2O4+CO2+H2O����4�����շ۳�ȥ���Է�ˮ�е��ظ�������ӣ�Cr2O72-��ת��ΪCr3+���ķ�Ӧ����ʽΪ��6H++Cr2O72-+ S2O42��== 2Cr3++ 2SO42��+3 H2O����ÿ����0.1mol���շۣ������Ͽ��Գ�ȥCr2O72-�����ʵ���Ϊ0.1 mol����5����������֪������ҺΪNa2S2O3��Һ�������м���ϡ��������������ơ��������������ˮ��������Ӧ�����ӷ���ʽΪS2O32-+2H+=SO2+S��+H2O�����շ۷ֽ�������������ơ��������ƺͶ�������ѧ����ʽΪ2 Na2S2O4 = Na2S2O3+Na2SO3+SO2����6�����շ��ڿ�������������������������������������Ӧ�ڣ�2Na2S2O4+O2+H2O=4NaHSO3+NaHSO4������ΪNaHSO3��NaHSO4�Ļ���Ҫ֤������ʱ�������Ǣڵķ�Ӧ���ɼ�������������ɣ�ʵ�鷽��Ϊ��ȡ������������ˮ�У�����BaCl2��Һ���а�ɫ������������֤���Ǣڣ�Ҳ������H++HSO3��==H2O+SO2�����ʵ�飬ʵ�鷽��Ϊ��ȡ������������ˮ�У����ŵ��̼�����ζ����֤���Ǣڡ�
���㣺�Ա��շ۵��Ʊ���Ӧ��Ϊ���忼�����ʽ����ѧ����ʽ����д������������Ʊ���������ԭ�ļ��㼰ʵ�鷽������ơ����ۡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�˲��и���5��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��2 L���ܱ������з�����ӦxA(g)��yB(g) zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ����
zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ����

A��200 ��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v(B)��0.04 mol��L��1��min��1
B��200��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ25 L2/mol2
C�������������200�潵�µ�100�棬ԭƽ��һ�����ƻ��������淴Ӧ���ʾ�����
D����ͼ�ҿ�֪����ӦxA(g)��yB(g) zC(g)�Ħ�H<0����a��2
zC(g)�Ħ�H<0����a��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ��У��ѧ�����п��Ը�һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
NA��ʾ�����ӵ�������ֵ�����������в���ȷ����
A��Fe���״����2.24LCl2ǡ����ȫ��Ӧ��ת�Ƶ�����ĿΪ0.2NA
B��0.5molNa2O2��0.5molNa2O��ɵĻ�����У�����������ĿΪ1.5NA
C��17gNH3�����к��еĹ��õ��Ӷ���Ϊ3NA
D��1.7gOH��������������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�����еڶ�ѧ�ڸ߶���ѧ���п��ԣ�B�����Ծ��������棩 ���ͣ�ѡ����
���б仯�У����Կ����ɼӳɷ�Ӧ������ǣ� ��
A. ��Ȳͨ��������������Һ�У���Һ��ɫ
B����ϩ��һ���¶ȡ�ѹǿ�ʹ����������£��ۺ�Ϊ����ϩ
C����һ�������£�������Ũ�����Ũ����Ļ��Һ�У�����״������
D���ڴ����������£���ϩ��ˮ��Ӧ�����Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�����еڶ�ѧ�ڸ߶���ѧ���п��ԣ�B�����Ծ��������棩 ���ͣ�ѡ����
���и��л���ķ����������ȷ���ǣ� ��
A���Լ����ӣ� �����ڷ����� B��
�����ڷ����� B�� 2-�һ�����
2-�һ�����
C�� 3-���� D��
3-���� D�� 3-��-1-��ϩ
3-��-1-��ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�����п����������ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A��ij�������ķ���ʽΪC10H14��������ʹ��ˮ��ɫ������ʹ����KMnO4��Һ��ɫ���ҷ��ӽṹ��ֻ��һ���������������������3��
B�� �� ת��Ϊ
ת��Ϊ �ķ����Ǽ���������NaOH��Һ�����ȣ� ��ͨ��������CO2
�ķ����Ǽ���������NaOH��Һ�����ȣ� ��ͨ��������CO2
C��1molij�л���Ľṹ��ʽΪ  ��ͨ����ȥ��Ӧ��ȥ1 molHClʱ���ܵõ� 5 �ֲ�ͬ��������������칹��
��ͨ����ȥ��Ӧ��ȥ1 molHClʱ���ܵõ� 5 �ֲ�ͬ��������������칹��
D���������ļ��顢��ϩ��1��3-����ϩ��C4H6���ֱ���ȼ�գ������������������μ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ������ѧ���������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
ijУ��ѧ��ȤС���ͬѧ�������ʵ�������Լ����Ҷ�к��иơ����������ֽ���Ԫ�ء�����֪��ȫ������pH��Ca(OH)2��pH �� 13��Al(OH)3��pH �� 5.5��Fe(OH)3��pH �� 4.1��
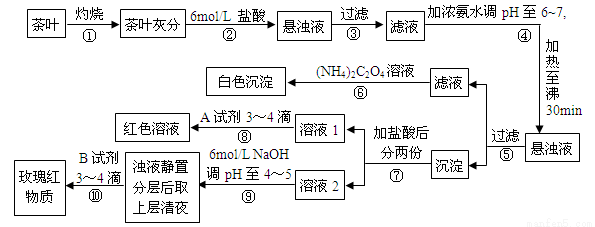
����˵������ȷ����
A������ڼ���6mol/L�������ҪĿ����Ϊ�˽���Ҷ�ҷ��еĸơ������������Ի�����ת��Ϊ�������Ȼ���
B�������������Һ�����ʵ���Ҫ�ɷ�Ϊ��CaCl2��NH3��H2O
C��������Լ����Ԫ�ش��ڣ����ӷ�Ӧ����ʽΪCa2++C2O42- = CaC2O4��
D���������A�Լ�ΪKSCN��Һ�����ӷ�Ӧ����ʽΪFe3++3SCN-  Fe(SCN)3
Fe(SCN)3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�����и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A��̫���ܵ�ذ����иߴ��赥�ʣ����ά����Ҫ�ɷ�Ҳ�ǹ�
B���������ͳ�Ʒ����������о���ʵ�鷽����ģ�ͻ��������ǻ�ѧ�о��ij��÷���
C���˴Ź����ס�������ס���������������ۺ����ã������ڷ����л���Ľṹ
D����ɫӫ�⵰�����о���֢�������ƵĹ�����Ӧ��ͻ���������Ի���������¿��ܻ�ʧȥ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㽭ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��8�֣���ij�л���A�ķ�����ṹ��ʽ����ͼ ����ش�
����ش�
��1��д���л���A�й����ŵ����ƣ�_______________��
��2��A������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ�ǣ�________________��
��3�������ӵ�A���Ȼ��ͷ��ǻ����Ӽ�ɻ��Ľṹ��ʽΪ ��
��4����AΪ���������Ȼ��ʹ��ǻ��γɸ߷������۲���ķ���ʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com