
(1)欲从苯酚的乙醇溶液中回收苯酚,有下列操作,合理的顺序是 (填字母)。
①蒸馏 ②过滤 ③静置分液 ④加入足量金属钠 ⑤通入过量CO2
⑥加入足量NaOH 溶液 ⑦加入足量FeCl3溶液 ⑧加入足量浓溴水
A. ⑧ ② B.⑥ ① ⑤ ③ C.④② D.⑦ ① ③
(2)下列说法正确的是 (填序号)。
①麦芽糖及其水解产物均能发生银镜反应,且试管内壁的银镜需用稀氨水洗涤
②蛋白质溶液中加入饱和硫酸铵溶液,有沉淀析出,加水后沉淀也不溶解
③淀粉液中加入几滴稀硫酸加热几分钟,冷却后加入银氨溶液并水浴加热,没有观察到银镜现象,证明淀粉未发生水解
④只用溴水就能鉴别四氯化碳、甲苯、乙烯、乙醇
Ⅱ已知:CH3CH2OH+NaBr+H2SO4(浓)  CH3CH2Br+NaHSO4 +H2O。
CH3CH2Br+NaHSO4 +H2O。
实验室制备溴乙烷(沸点为38.4℃)的装置如图:圆底烧瓶中加入10mL95%乙醇、28mL浓硫酸,然后加入研细的10.3g溴化钠和几粒碎瓷片,小火加热,使NaBr充分反应。
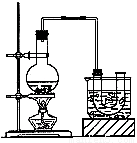
(1)反应时若温度过高会降低溴乙烷的产率,原因是 ;也可看到有红棕色气体产生,该气体的化学式为 。为避免温度过高,宜采用 加热。
(2)反应结束后,U形管中粗制的溴乙烷呈棕黄色。为了除去其中的杂质,最好选用下列试剂中的
(填序号)。
A.Na2SO3溶液 B.H2O C.NaOH溶液 D.CCl4
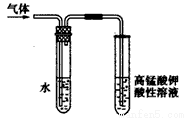
(3)溴乙烷在NaOH水溶液和NaOH乙醇溶液发生不同类型的反应,生成不同的产物,用右图所示装置进行实验:该实验的目的是 。 盛水的试管(装置)的作用是 。
(4)为检验溴乙烷中的溴元素,正确的操作顺序是:取少量溴乙烷,然后 (填序号)。
①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液 ⑤冷却
(5)经提纯最终得到纯净的溴乙烷为7.63g,则溴乙烷的产率为 (保留两位有效数字)。
科目:高中化学 来源:2016届湖北省沙市高三下高考第一次模拟理综化学试卷(解析版) 题型:填空题
研究发现,NOx和SO2是雾霾的主要成分。
(一)NOx主要来源于汽车尾气。
已知:N2(g)+O2(g) 2NO(g) △H=+180.50 kJ·mol-1
2NO(g) △H=+180.50 kJ·mol-1
2CO(g)+O2(g) 2 CO2(g) △H=-566.00kJ·mol-1
2 CO2(g) △H=-566.00kJ·mol-1
(1)为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环。写出该反应的热化学方程式________。
(2)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0-15min)中NO的物质的量随时间变化如右图所示。①T℃时该化学反应的平衡常数K=_________;平衡时若保持温度不变,再向容器中充入CO、N2各0.8 mol,平衡将_______移动。(填“向左”、“向右”或“不”)

②图中a、b分别表示在一定温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是__________。(填“a”或“b”)
③15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是______。
(二)SO2主要来源于煤的燃烧。燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。
(3)用纯碱溶液吸收SO2可将其转化为HSO3-。该反应的离子方程式是_____________。
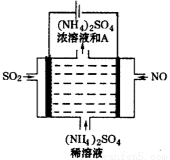
(4)下图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。
①写出物质A的化学式________,阳极的电极反应式是_______。
②该电解反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高一下期中化学试卷(解析版) 题型:填空题
有一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是_________,用电子式表示XY2的形成过程 X与氢元素形成的化合物的电子式是_______________。
(2)主族元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是________;D与E能形成一种分子,该分子的结构式为__________________;D所在族元素的氢化物中,沸点最低的是(填名称)_________;X与E形成的离子化合物 XE2中 (填“有”“无”)共价键。
(3)短周期元素W与Y同周期,其单质是半导体材料;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是_________。
(4)用化学式回答:①D与Y的氢化物稳定性 _>______ ;
;
②最高价氧化物对应水化物酸性 _> ____。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高一下期中化学试卷(解析版) 题型:选择题
对于10mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是( )
①升高温度; ②改用10mL 3mol/L盐酸; ③改用30mL 1mol/L醋酸;
④用等量锌粉代替锌粒; ⑤改用10mL 3mol/L硝酸;
A.①②④ B.①③④⑤ C.①②③④ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高一下期中化学试卷(解析版) 题型:选择题
能源是当今社会发展的三大支柱之一。有专家预测氢能源将是未来最理想的新能源,而最理想的氢的循环模式如图,此循环可以节约原料,缓解能源危机。在此构想的物质循环中太阳能最终转化为( )
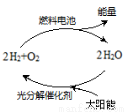
A.化学能 B. 热能 C. 生物能 D. 电能
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期中化学试卷(解析版) 题型:选择题
草酸二酯(CPPO)结构简式如右图,下列说法正确的是( )
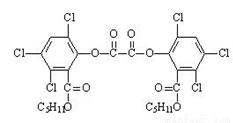
A.草酸二酯的分子式为C26H22Cl6O8
B.1mol草酸二酯与氢氧化钠稀溶液反应时(苯环上卤素不水解),最多消耗6mol NaOH
C.草酸二酯酸性条件下水解可以得到两种有机物
D.1mol草酸二酯与氢气完全反应,需要氢气10mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二下期中化学试卷(解析版) 题型:选择题
下列各组物质不属于同分异构体的是 ( )
A.2,2-二甲基-1-丙醇和2-甲基-2-丁醇 B.苯甲醇和对甲基苯酚
C.2-甲基丁烷和戊烷 D.乙二醇和丙三醇
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东实验中学高二下期中化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.C—O键的极性比N—O键的极性大
B.CO和N2互为等电子体,且N2的沸点比CO的高
C.H2CO3、H2SiO3、H3PO4酸性越来越弱
D.金属K采用面心立方堆积,空间利用率为74%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期中化学试卷(解析版) 题型:选择题
电解质量分数为5.2%的NaOH溶液1 L(密度为1.06 g/cm3),用铂作电极电解,当溶液中NaOH的质量分数改变了1.0% 时停止电解,此时溶液中符合下表关系的是( )
NaOH的质量分数 | 阳极析出物质的质量/g | 阴极析出物质的质量/g | |
A | 6.2% | 19 | 152 |
B | 6.2% | 152 | 19 |
C | 4.2% | 1.2 | 9.4 |
D | 4.2% | 9.4 | 1.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com