
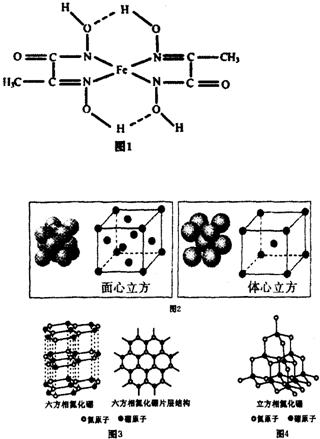
分析 (1)Fe原子的电子排布式是1s22s22p63s23p63d64s2,与铁同周期的所有副族元素的基态原子中,最外层电子数与铁相同的元素的3d轨道电子数为1、2、3、5、10;
(2)①非金属性越强,元素的电负性越大;
②化合物中形成C=N双键的N原子形成2个σ键,含有1对孤电子对,而形成单键的N原子,形成2个σ键,含有2对孤电子对,杂化轨道数目分别为3、4;
③C=N双键的N原子有1对孤对电子与亚铁离子之间形成配位键,另外N原子带1个单位负电荷,与亚铁离子之间形成离子键;
(3)利用均摊法计算晶胞中Fe原子个数;根据密度公式ρ=$\frac{\frac{M}{NA}×Fe原子个数}{V}$;
(4)①六方相氮化硼晶体层内一个硼原子与相邻氮原子形成3个共价单键,该物质的层状结构中不存在自由移动的电子;
②氮化硼与碳元素的单质相似,结合金刚石的结构进行判断,立方相氮化硼晶体中,每个硼原子连接12个六元环,在地壳内部,离地面越深,其压强越大、温度越高.
解答 解:(1)Fe原子的电子排布式是1s22s22p63s23p63d64s2,与铁同周期的所有副族元素的基态原子中,最外层电子数与铁相同的元素的3d轨道电子数为1、2、3、5、10,还有5种,
故答案为:5;
(2)①非金属性越强,元素的电负性越大,则电负性O>N>C>H>Fe,
故答案为:O>N>C>H>Fe;
②化合物中形成C=N双键的N原子形成2个σ键,含有1对孤电子对,而形成单键的N原子,形成2个σ键,含有2对孤电子对,杂化轨道数目分别为3、4,N原子采取sp2、sp3杂化,
故答案为:sp2、sp3;
③C=N双键的N原子有1对孤对电子与亚铁离子之间形成配位键,另外N原子带1个单位负电荷,与亚铁离子之间形成离子键,标出亚铁离子的配位键为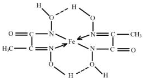 ,
,
故答案为:
(3)利用均摊法计算晶胞中Fe原子个数,面心立方晶胞中Fe原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4、体心立方晶胞中Fe原子个数=1+8×$\frac{1}{8}$=2,
所以二者Fe原子个数之比=4:2=2:1;
设Fe原子半径为rcm,面心立方晶胞半径=2$\sqrt{2}$rcm,其体积=(2$\sqrt{2}$rcm)3,体心立方晶胞半径=$\frac{4\sqrt{3}}{3}$rcm,体积=($\frac{4\sqrt{3}}{3}$rcm)3,
其密度之比=$\frac{\frac{M}{NA}×4}{(2\sqrt{2}rcm)^{3}}$:$\frac{\frac{M}{NA}×2}{(\frac{4\sqrt{3}}{3}rcm)^{3}}$=4$\sqrt{2}$:3$\sqrt{3}$,
故答案为:2:1;4$\sqrt{2}$:3$\sqrt{3}$;
(4)①六方相氮化硼晶体层内一个硼原子与相邻氮原子形成3个共价单键,六方相氮化硼晶体内B-N键数与硼原子数之比为3:1,该物质的层状结构中不存在自由移动的电子,所以不导电,
故答案为:3:1;立方氮化硼晶体内无自由移动的电子;
②氮化硼与金刚石的结构相似,立方相氮化硼晶体中,每个硼原子连接12个六元环,在地壳内部,离地面越深,其压强越大、温度越高,根据题干知,实验室由六方相氮化硼合成立方相氮化硼需要的条件应是高温高压,
故答案为:12;高温、高压.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、杂化方式、配合物、晶胞计算等,配位键判断为易错点,掌握均摊法进行晶胞计算,需要学生具备一定的数学计算能力,侧重考查学生分析计算及空间想象能力,注意Fe晶胞面心立方和体心立方区别,题目有一定难度.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 ⑦CH3CH2OH中与甲烷互为同系物的是①,分子空间构型为平面形的是④⑥,直线形的是⑤.
⑦CH3CH2OH中与甲烷互为同系物的是①,分子空间构型为平面形的是④⑥,直线形的是⑤.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 相关信息 | |
| A | 所处的周期数、族序数分别与其原子序数相等 |
| B | 原子核外电子有4种不同的运动状态 |
| C | 元素原子的核外成对电子数是未成对电子数的2倍且有3个能级 |
| D | 元素原子的核外p电子数比s电子数少1 |
| E | E原子的第一至第四电离能如下:I1=738 kJ•mol-1 I2=1451 kJ•mol-1 I3=7733 kJ•mol-1 I4=10540 kJ•mol-1 |
| F | 第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满 |
 ,该同学所画的电子排布图违背了泡利原理.
,该同学所画的电子排布图违背了泡利原理.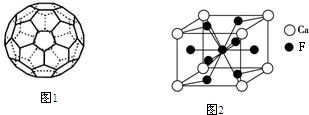
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在化合物中呈+1价 | |
| B. | 常温下,单质能与水剧烈反应产生H2 | |
| C. | 氢氧化铯为强碱 | |
| D. | 铯元素的金属性比钠元素的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl溶液 | B. | 溴水 | C. | 酸性KMnO4溶液 | D. | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
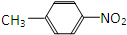 和
和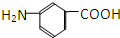 E.35Cl和37Cl
E.35Cl和37Cl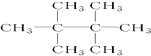 ,
,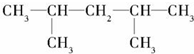 ,该烯烃可能的结构简式有2种.
,该烯烃可能的结构简式有2种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com