
| A. | 将稀硫酸改成浓硫酸 | B. | 滴加少量硫酸钠溶液 | ||
| C. | 硫酸改成4 mol•L-1的醋酸 | D. | 滴加几滴硫酸铜溶液 |
分析 A、金属锌和浓硫酸之间反应不会产生氢气;
B、滴加少量硫酸钠溶液,相当于该硫酸溶液中加入水,硫酸的浓度减少;
C、硫酸改成4 mol•L-1的醋酸,氢离子浓度增加;
D、滴加几滴硫酸铜溶液,金属锌会置换出金属铜,形成锌、铜、硫酸原电池.
解答 解:A、将稀硫酸改成浓硫酸,金属锌和浓硫酸之间反应不会产生氢气,故A错误;
B、滴加少量硫酸钠溶液,相当于该硫酸溶液中加入水,硫酸的浓度减少,因减少反应物的浓度,反应速率减慢,故B错误;
C、硫酸改成4 mol•L-1的醋酸,氢离子浓度增加,所以速率加快,故C正确;
D、滴加几滴硫酸铜溶液,金属锌会置换出金属铜,形成锌、铜、硫酸原电池,加快反应速率,故D正确.
故选CD.
点评 本题较简单,考查影响化学反应速率的常见因素如:温度、浓度、构成原电池、增大接触面等,但浓硫酸的性质是学生解答中容易忽略的知识.浓硫酸与金属反应得不到氢气.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 向漂粉精溶液中通入过量的二氧化碳:ClO-+H2O+CO2═HClO+HCO3- | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 二氧化锰与浓盐酸反应:MnO2+4H++4Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+2Cl2↑, | |
| D. | 碳酸钙粉末与新制氯水反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①②③ | C. | ③④⑤ | D. | ①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
时间/min n(CH4)/mol 温度 | 0 | 10 | 20 | 40 | 50 |
| T1 | 1.00 | 0.70 | 0.50 | 0.20 | 0.20 |
| T2 | 1.00 | 0.60 | 0.36 | … | 0.30 |
| A. | 10 min内,T1时的化学反应速率比T2时大 | |
| B. | 温度:T1<T2 | |
| C. | Q>0 | |
| D. | 化学平衡常数:K(T1)<K(T2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
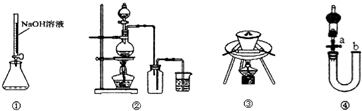
| A. | 用装置①量取15.00mL的NaOH溶液 | |
| B. | 用装置②制备并收集Cl2 | |
| C. | 用装置③陶瓷坩埚高温煅烧CaCO3固体 | |
| D. | 关闭活塞a,从b处加水,以检查装置④的气密性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①②③④ | C. | ①②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
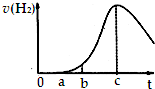 把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )| A. | 曲线由0→a段发生了氧化还原反应 | |
| B. | 曲线由b→c段,产生氢气的速率增加较快的主要原因是反应放热 | |
| C. | c点达到了平衡 | |
| D. | c点以后,反应逐渐消耗了产生的氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶液 | 加入的物质 | 答案序号 |
| AlCl3溶液 | 通入过量的NH3 | ① |
| 含少量NaOH的NaAlO2溶液 | 通过量的CO2 | ② |
| NaAlO2溶液 | 滴加稀H2SO4至过量 | ③ |
| MgCl2和AlCl3的混合液 | 滴加NaOH溶液至过量 | ④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com