
| A. | 5.6 g铁与足量的氯气反应失去的电子为0.2 mol | |
| B. | 25℃、pH=0的溶液中,Al3+、NH4+、NO3-、Fe2+可以大量共存 | |
| C. | 2Fe3++Fe═3Fe2+成立说明氧化性:Fe3+>Fe2+ | |
| D. | 硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+═Fe3++4H2O |
分析 A.氯气与铁反应生成氯化铁,1mol的铁转移3mol的电子;
B.pH=0的溶液中存大大量的氢离子,H+、NO3-、Fe2+发生氧化还原反应;
C.氧化剂的氧化性大于氧化产物的氧化性;
D.电荷不守恒.
解答 解:A.5.6 g铁的物质的量为0.1 mol与足量的氯气反应失去的电子为0.3 mol,故A错误;
B.pH=0的溶液中存大大量的氢离子,H+、NO3-、Fe2+发生氧化还原反应,三者不能大量共存,故B错误;
C.2Fe3++Fe═3Fe2+反应中三价铁离子为氧化剂,二价铁离子为氧化产物,所以氧化性:Fe3+>Fe2+,故C正确;
D.硫酸亚铁溶液中加入过氧化氢溶液反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,故D错误;
故选C.
点评 本题考查了元素化合物知识,为高频考点,侧重于学生的分析、计算能力的考查,明确铁及其化合物的性质是解题关键,注意A选项,氯气不足,转移电子数应依据氯气的量计算.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗硅 $→_{高温}^{Cl_{2}}$ SiCl4$→_{高温}^{H_{2}}$Si | |
| B. | Mg(OH)2$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$ Mg、 | |
| C. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(aq)$\stackrel{蒸发}{→}$无水FeCl3 | |
| D. | AgNO3(aq) $\stackrel{NH_{3}•H_{2}O}{→}$[Ag(NH3)2]OH(aq) $→_{△}^{蔗糖}$ Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH>7的溶液一定是碱溶液 | |
| B. | pH试纸先用水润湿不一定会对测定结果造成偏差 | |
| C. | pH试纸应不经润湿直接放入待测液中 | |
| D. | 将酚酞溶液滴加到pH<7的溶液中会变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用100mL量筒取5.0mL稀硫酸 | |
| B. | 用托盘天平准确称取2.50gNaCl固体 | |
| C. | 实验室制取蒸馏水的装置中,温度计水银球应插入蒸馏烧瓶液面以下 | |
| D. | 配制240mL0.1mol/LNaOH溶液应该选择250mL的容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
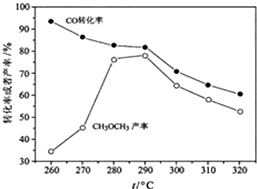 二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应:
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雪白、漂亮的“白木耳”,可能是在用硫黄熏制的过程中产生的SO2所致 | |
| B. | 钢铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| C. | 绿色化学的核心是从源头上消除工业生产对环境的污染 | |
| D. | 硅胶可用作食品干燥剂和催化剂载体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com