
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为;
(2)反应是反应.(选填“吸热”、放热).
(3)能判断该反应是否达到化学平衡状态的依据是 .
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(CH2)=c(CO)c(H2O),试判断此时的温度为℃
【答案】
(1)![]()
(2)吸热
(3)bc
(4)830
【解析】解:(1)因平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以 ![]() ,故答案为:
,故答案为: ![]() ;(2)化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热,故答案为:吸热;(3)a、反应是一个反应前后体积不变的反应,压强的改变不会要引起平衡移动,故a错误;
;(2)化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热,故答案为:吸热;(3)a、反应是一个反应前后体积不变的反应,压强的改变不会要引起平衡移动,故a错误;
b、化学平衡时,各组分的浓度不随时间的改变而改变,故b正确;
c、化学平衡状态的标志是v正=v逆 , 所以v正(H2)=v逆(H2O)表明反应达到平衡状态,故c正确;
d、c(CO2)=c(CO)时,不能表明正逆反应速率相等,不一定达到了平衡状态,故d错误.
故选bc;(4)平衡浓度符合下式c(CO2)c(CH2)=c(CO)c(H2O)时,浓度熵和平衡常数相等均等于1,平衡常数只受温度的影响,当K=1时,根据表中数据,所以温度是830℃,
故答案为:830.
(1)根据化学平衡常数的概念来书写;(2)根据温度对化学平衡、化学平衡常数的影响来回答;(3)化学平衡状态的标志:正逆反应速率相等;(4)根据浓度熵和平衡常数的关系来回答.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2 . 某同学在实验室中对NH3与NO2反应进行了探究.回答下列问题:
(1)氨气的制备 
①氨气的发生装置可以选择上图中的 , 反应的化学方程式为 .
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→(按气流方向,用小写字母表示).
(2)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度下按图示装置进行实验.
操作步骤 | 实验现象 | 解释原因 |
打开K1 , 推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中 | ②反应的化学方程式 |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
打开K2 | ③ | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子反应可用H++OH-= H2O表示的是( )
A. 氢氧化钡和硫酸 B. 氢氧化铜和盐酸
C. 盐酸和氢氧化钠 D. 硫酸和氢氧化镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:MnO2熔融氧化:3MnO2+KClO3+6KOH ![]() 3K2MnO4+KCl+3H2O;K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3 . 已知K2MnO4溶液显绿色.请回答下列问题:
3K2MnO4+KCl+3H2O;K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3 . 已知K2MnO4溶液显绿色.请回答下列问题:
(1)MnO2熔融氧化应放在中加热(填仪器编号).①烧杯②瓷坩埚③蒸发皿④铁坩埚
(2)在MnO2熔融氧化所得产物的热浸取液中通入CO2气体,使K2MnO4歧化的过程在如图装置中进行,A、B、C、D、E为旋塞,F、G为气囊,H为带套管的玻璃棒.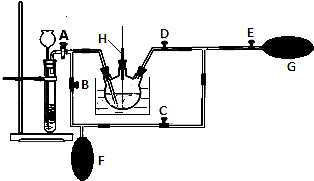
①为了能充分利用CO2 , 装置中使用了两个气囊.当试管内依次加入块状碳酸钙和盐酸后,关闭旋塞B、E,微开旋塞A,打开旋塞C、D,往热K2MnO4溶液中通入CO2气体,未反应的CO2被收集到气囊F中.待气囊F收集到较多气体时,关闭旋塞 , 打开旋塞 , 轻轻挤压气囊F,使CO2气体缓缓地压入K2MnO4溶液中再次反应,未反应的CO2气体又被收集在气囊G中.然后将气囊G中的气体挤压入气囊F中,如此反复,直至K2MnO4完全反应.
②检验K2MnO4歧化完全的实验操作是 .
(3)将三颈烧瓶中所得产物进行抽滤,将滤液倒入蒸发皿中,蒸发浓缩至 , 自然冷却结晶,抽滤,得到针状的高锰酸钾晶体.本实验应采用低温烘干的方法来干燥产品,原因是 .
(4)利用氧化还原滴定法进行高锰酸钾纯度分析,原理为:2MnO4﹣+5C2O42﹣+16H+=2Mn2++10CO2↑+8H2O现称取制得的高锰酸钾产品7.245g,配成500mL溶液,用移液管量取25.00mL待测液,用0.1000molL﹣1草酸钠标准溶液液进行滴定,终点时消耗标准液体积为50.00mL(不考虑杂质的反应),则高锰酸钾产品的纯度为(保留4位有效数字,已知M(KMnO4)=158gmol﹣1).若移液管用蒸馏水洗净后没有用待测液润洗或烘干,则测定结果将(填“偏大”、“偏小”、“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.Si投入NaOH溶液中Si+2OH﹣═SiO ![]() +H2
+H2
B.把Al中投入到少量氢氧化钠溶液Al3++3OH﹣═Al(OH)3↓
C.向明矾水溶液中滴加氢氧化钡溶液,恰好使“SO42﹣”完全沉淀:Al3++2SO ![]() +2Ba2++2OH﹣═2BaSO4↓+Al(OH)3
+2Ba2++2OH﹣═2BaSO4↓+Al(OH)3
D.Na[Al(OH)4]溶液中加入过量的CO2:[Al(OH)4]﹣+CO2═HCO ![]() +Al(OH)3↓
+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将![]() 明矾溶于水形成100mL溶液,以下说法正确的是
明矾溶于水形成100mL溶液,以下说法正确的是![]()
A. 明矾净水是利用了明矾的强氧化性
B. 溶液的焰色反应为紫色,这是化学性质
C. 加入![]() 溶液至沉淀物质的量达到最大,消耗
溶液至沉淀物质的量达到最大,消耗![]() 溶液
溶液![]()
D. 加入![]() 溶液至
溶液至![]() 恰好完全沉淀,
恰好完全沉淀, ![]() 全部转化为
全部转化为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两组物质:①CO2、P2O5、CaO、SO2,②O2、Mg、Zn、Al。每组中有一种物质在某些化学性质或分类上与其他几种物质不同,这两种物质是①_______________,②_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com