
【题目】在T℃时,发生反应C(s)+H2O(g) ![]() CO(g)+H2(g)。
CO(g)+H2(g)。
(1)T℃时,在一个2L的密闭容器中加入4molC和1molH2O(g),5min后反应达到平衡,C的转化率为20%。
①0~5min内,用H2O(g)表示的平均反应速率为____________。
②该反应达到平衡的标志是______。
a.气体的平均相对分子质量不变
b.气体的密度不变
c.H2O(g)、CO(g)、H2(g)的物质的量之比为1:1:1
d.气体的总物质的量不变
(2)T℃时,在下列密闭容器中加入相应的物质进行实验,中间的隔板可以自由滑动。

①若左室中气体的平均相对分子质量一直保持不变,则反应开始前H2O(g)、H2(g)的物质的量之比是__________。
②反应在达到平衡时,中间的隔板所处的位置是________。
a.1~1.5之间 b.1.5处 c.1.5~2之间
(3)已知:I.破坏1mol共价键所需要的能量如下表:
共价键 | 石墨中的碳碳键 | H-H | C≡O | H-O |
能量/kJ | 475.7 | 436 | 1072 | 463 |
Ⅱ.石墨层由六角形蜂巢结构的碳原子构成,如图所示:
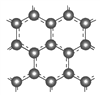
某同学构想:通过下列装置实现C(s)+H2O(g) ![]() CO(g)+H2(g)的反应。
CO(g)+H2(g)的反应。
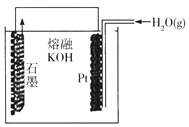
①按该考生的构想,石墨电极发生的反应式为_______________。
②这个构想成立吗?说明理由: _______________。
【答案】 0.08 mol/(L·min) abd 5:3 a C-2e- +2OH-=CO↑+H2O 不成立。因为根据反应C(s)+H2O(g) ![]() CO(g) +H2(g),物质的断键和成键的能量变化是:1.5×475.7 kJ +2×463 kJ -1072 kJ - 436 kJ=+131.5 kJ>0,说明是吸热反应,不能将化学能转化为电能
CO(g) +H2(g),物质的断键和成键的能量变化是:1.5×475.7 kJ +2×463 kJ -1072 kJ - 436 kJ=+131.5 kJ>0,说明是吸热反应,不能将化学能转化为电能
【解析】试题分析:本题考查化学反应速率的计算,化学平衡的标志,化学平衡的计算和极限法,电极反应式的书写,反应热的计算。
(1)①C的转化率为20%,转化C的物质的量为4mol![]() 20%=0.8mol,则转化H2O(g)的物质的量为0.8mol,υ[H2O(g)]=0.8mol
20%=0.8mol,则转化H2O(g)的物质的量为0.8mol,υ[H2O(g)]=0.8mol![]() 2L
2L![]() 5min=0.08mol/(L·min)。
5min=0.08mol/(L·min)。
② a项,反应生成的CO和H2的物质的量之比为1:1,反应生成的CO和H2的平均相对分子质量为15(28![]() 1/2+2
1/2+2![]() 1/2=15),建立平衡的过程中气体的平均相对分子质量减小,平衡时气体的平均相对分子质量不变,气体的平均相对分子质量不变表明反应达到平衡状态;b项,建立平衡过程中气体的质量增大,容器体积不变,气体的密度增大,平衡时气体的质量不变,气体的密度不变,气体的密度不变表明反应达到平衡状态;c项,平衡时各物质的浓度不再变化,不一定等于化学计量数之比,H2O(g)、CO(g)、H2(g)的物质的量之比为1:1:1不能说明反应一定达到平衡状态;d项,该反应的正反应为气体分子数增大的反应,建立平衡过程中气体物质的量增大,平衡时气体物质的量不变,气体的总物质的量不变说明反应达到平衡状态;能说明反应达到平衡的标志是abd。
1/2=15),建立平衡的过程中气体的平均相对分子质量减小,平衡时气体的平均相对分子质量不变,气体的平均相对分子质量不变表明反应达到平衡状态;b项,建立平衡过程中气体的质量增大,容器体积不变,气体的密度增大,平衡时气体的质量不变,气体的密度不变,气体的密度不变表明反应达到平衡状态;c项,平衡时各物质的浓度不再变化,不一定等于化学计量数之比,H2O(g)、CO(g)、H2(g)的物质的量之比为1:1:1不能说明反应一定达到平衡状态;d项,该反应的正反应为气体分子数增大的反应,建立平衡过程中气体物质的量增大,平衡时气体物质的量不变,气体的总物质的量不变说明反应达到平衡状态;能说明反应达到平衡的标志是abd。
(2)①设反应开始前H2O(g)、H2(g)物质的量依次为xmol、ymol,转化H2O(g)物质的量为amol,用三段式
C(s)+H2O(g) ![]() CO(g)+H2(g)
CO(g)+H2(g)
n(起始)(mol) x 0 y
n(转化)(mol) a a a
n(某时刻)(mol) x-a a y+a
左室中气体的平均相对分子质量一直保持不变, ![]() =
=![]() ,解得x:y=5:3,反应开始前H2O(g)、H2(g)物质的量之比为5:3。
,解得x:y=5:3,反应开始前H2O(g)、H2(g)物质的量之比为5:3。
②设反应开始前H2O(g)、H2(g)物质的量依次为xmol、ymol,起始到平衡转化H2O(g)物质的量为bmol,用三段式
C(s)+H2O(g) ![]() CO(g)+H2(g)
CO(g)+H2(g)
n(起始)(mol) x 0 y
n(转化)(mol) b b b
n(平衡)(mol) x-b b y+b
根据同温同压下气体体积之比等于气体物质的量之比,反应前(x+y):n(N2)=1:2,x的最大值为n(N2)/2;反应达到平衡时,左室气体物质的量为x+y+b,由于是可逆反应则0![]() b
b![]() x,左室反应达平衡时气体物质的量x+y
x,左室反应达平衡时气体物质的量x+y![]() x+y+b
x+y+b![]() x+y+x,左室气体物质的量n(N2)/2
x+y+x,左室气体物质的量n(N2)/2![]() x+y+b
x+y+b![]() n(N2),右室N2物质的量不变,根据同温同压下气体体积之比等于气体物质的量之比,左室达平衡时隔板所处位置在1~1.5之间,答案选a。
n(N2),右室N2物质的量不变,根据同温同压下气体体积之比等于气体物质的量之比,左室达平衡时隔板所处位置在1~1.5之间,答案选a。
(3)①反应中C元素的化合价由0价升至CO中的+2价,石墨电极发生失电子的氧化反应,电极反应式为C(s)-2e-+2OH-=CO↑+H2O。
②根据石墨的结构,1mol石墨中含碳碳键1.5mol,反应C(s)+H2O(g) ![]() CO(g)+H2(g)的ΔH=反应物的键能总和-生成物的键能总和=1.5E(碳碳键)+2E(H-O)-E(C
CO(g)+H2(g)的ΔH=反应物的键能总和-生成物的键能总和=1.5E(碳碳键)+2E(H-O)-E(C![]() O)-E(H-H)=1.5
O)-E(H-H)=1.5![]() 475.7kJ/mol+2
475.7kJ/mol+2![]() 463kJ/mol-1072kJ/mol-436kJ/mol=+131.55kJ/mol,该反应为吸热反应,不能通过原电池将化学能转化成电能,构想不成立。
463kJ/mol-1072kJ/mol-436kJ/mol=+131.55kJ/mol,该反应为吸热反应,不能通过原电池将化学能转化成电能,构想不成立。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[一lg c(M2+)]与溶液pH的变化关系如图所示,已知该温度下,Ksp[Cu(OH)2]2],下列说法正确的是 ( )

A. b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1
B. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中:C(Fe2+):C(Cu2+):1:104.6
C. 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液
D. 除去CuSO4溶液中含有的少量Fe2+,可加入适量Cu0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁黄是一种重要的颜料,化学式为Fe2O3xH2O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含Fe2O3及少量的CaO、MgO等) 和黄铁矿粉(主要成分为FeS2) 制备铁黄的流程如下。
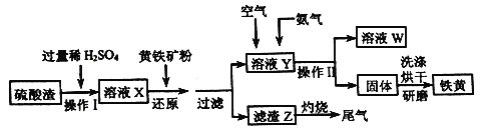
回答下列问题:
(1)操作I中为了提高硫酸渣的溶解速率,可采取的措施有_________(答两条即可)。
(2)溶液X中含有的金属离子有Fe3+和_____;溶液X中加入黄铁矿粉后,先发生反应FeS2+H2SO4( 稀)=FeSO4+ H2S↑+S↓,H2S 再将Fe3+还原,其离子方程式为_________。
(3)在溶液Y 中通入空气的目的是______________,再通入NH3后可观察到的现象是__________,若通入NH3后溶液的pH 过高,会影响产品纯度,原因是_________。
(4)操作II中除用到玻璃棒外,还需要的玻璃仪器是________。
(5)若将滤渣Z灼烧产生的尾气通入溶液X 中,充分反应后溶液的pH____(填“增大”、“减小”或“不变”)。
(6)为了测定所制备铁黄Fe2O3xH2O中x的值,用分析天平准确称量m1g样品置于坩埚中加热、冷却后称量;经过重复操作,当达到恒重时,残留固体质量为m2g,则x =______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用如图装置对电解质溶液导电性进行实验探究。下列说法中正确的是( )

A. 闭合开关K,电流计指针发生偏转,证明HCl溶液是电解质
B. 闭合开关K,向烧杯中加入NaCl固体,由于HCl与NaCl不反应,故电流计指针不发生变化
C. 闭合开关K,向溶液中加入CaCO3固体,电流计示数不变
D. 选取相同浓度的硫酸替换0.1 mol·L-1的HCl溶液,电流计的示数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年12月,华为宣布: 利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LixC6+Li1-xCoO2![]() C6+LiCoO2,其工作原理如图所示。下列关于该电池的说法不正确的是
C6+LiCoO2,其工作原理如图所示。下列关于该电池的说法不正确的是

A. 该电池若用隔膜可选用质子交换膜
B. 石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
C. 充电时,LiCoO2极 发生的电极反应为: LiCoO2-xe-=Li1-xCoO2+xLi+
D. 废旧的该电池进行“放电处理”让Li+从石墨烯中脱出而有利于回收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10mL0.1mol/LCaCl2溶液中滴加0.mol/L的Na2CO3溶液,滴加过程中溶液中-1gc(Ca2+)与Na2CO3溶液体积(V)的关系如图所示,下列有关说法正确的是

A. Ksp(CaCO3)=5×10-10
B. Z点对应的分散系很稳定
C. W、x、y三点中,水的电离程度最大的为y点
D. 若用等浓度的Na2SO4溶液代替Na2CO3溶液,则图像在x点后的变化如虚线部分所示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N、P、As的化合物在研究和生产中有许多重要用途。
(1)基态As原子的核外电子排布式为_________。
(2)N的第一电离能比O大,原因是______________。
(3)NH4+中H-N-H的键角比NH3中H-N-H 的键角_______(填“大”或“小”),原因是____________。
(4)K3AsO4中含有的化学键类型包括________;AsO43- 的空间构型为______。As4O6的分子结构如图1所示,则该化合物中As的杂化方式是__________。
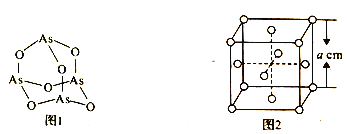
(5)化合物NH5中的所有原子最外层都满足稳定结构,则NH5 是_______晶体。
(6)白磷(P4)的晶体属于分子晶体,其晶胞结构如图2 (小圆圈表示白磷分子)。已知晶胞的边长为acm,阿伏加德罗常数的数值为NA,则该晶胞中含有P 原子的个数为______,该晶体的密度为_________(用含NA、a 的代数式表示) g.cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个圆所构成的元素概念的关系图,其中4为最大圆,3、2、1依次减小。试判断符合这种关系的是

A. 1.最基本元素、2.基本元素、3.主要元素、4.大量元素
B. 1.大量元素、2.主要元素、3.基本元素、4.最基本元素
C. 1.基本元素、2.最基本元素、3.大量元素、4.主要元素
D. 1.主要元素、2.大量元素、3.最基本元素、4.基本元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿水青山就是金山银山”。下列做法不利于保护环境的是( )
A.推广使用电动汽车等低碳交通工具
B.推广垃圾分类,电子设备以旧换新
C.用生物方法脱除生活污水中的氮和磷
D.加大铅酸蓄电池、含汞锌锰等电池的生产
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com