
铁及其化合物是中学化学中的一类重要物质,下列关于铁元素的叙述中正确的是( )
A.反应2Fe3++Fe===3Fe2+能够发生说明氧化性:Fe3+>Fe2+
B.25 ℃,pH=0的溶液中,Al3+、NH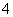 、NO
、NO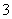 、Fe2+可以大量共存
、Fe2+可以大量共存
C.5.6 g铁与足量的氯气反应失去电子为0.2 mol
D.硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+===Fe3++4H2O
科目:高中化学 来源: 题型:
实验室利用如右图装置进行中和热的测定。
 回答下列问题:①如图装置中,为了酸碱能更充分地反应,应该增加一个 (填玻璃仪器名称);大烧杯上没有盖上硬纸板,测得的中和热数值将会 (填“偏大”、“偏小”或“无影响”)。
回答下列问题:①如图装置中,为了酸碱能更充分地反应,应该增加一个 (填玻璃仪器名称);大烧杯上没有盖上硬纸板,测得的中和热数值将会 (填“偏大”、“偏小”或“无影响”)。
②在操作正确的前提下提高中和热测定的准确性的关键是 ( 填代号)
A.进行实验时的气温
B.装置的保温隔热效果
C.实验所用酸碱溶液的体积
③如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将
(填“偏大”、“偏小”、“不变”);原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组以甲苯为主要原料,合成医药中间体F和Z。
②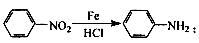 苯胺中氨基易被氧化。
苯胺中氨基易被氧化。
请回答下列问题:
(1)有机物A的结构简式为 。
(2)下列有关F的说法正确的是 。
a.分子式是C7H7NO2Br b.能形成内盐
c.能发生酯化反应和缩聚反应 d.1 mol的F最多可以和2 mol NaOH反应
(3)B→C的化学方程式是 。在合成F的过程中,B→C步骤不能省略,理由是 。
(4)写出同时符合下列条件的Z的同分异构体(不含Z,不考虑立体异构)。
①含有苯环结构 ②与Z含有相同官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
无水氯化铝是一种重要的催化剂,工业上由Al2O3制备无水氯化铝的反应为2Al2O3(s)+6Cl2(g)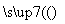 4AlCl3(g)+3O2(g) ΔH>0。下列分析错误的是( )
4AlCl3(g)+3O2(g) ΔH>0。下列分析错误的是( )
A.增大反应体系的压强,反应速率加快
B.加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量
C.电解熔融的Al2O3和AlCl3均能得到单质铝
D.将AlCl3·6H2O在氯化氢气流中加热,也可制得无水氯化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
将一浅绿色溶液,置于空气中,变黄色。将此黄色溶液逐滴滴入沸水中,形成一种红褐色胶体,下列说法中错误的是( )
A.该浅绿色溶液中含有Fe2+,在空气中被氧化为Fe3+
B.欲检验该黄色溶液中是否含有未被氧化的Fe2+,向其中滴加KSCN溶液
C.配制该浅绿色溶液,要向其中加少量酸与铁粉,目的是为了防止Fe2+的水解与氧化
D.欲检验浅绿色溶液中是否含有Fe3+,滴入KSCN溶液,看是否变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
常温常压下为无色液体,而且密度大于水的是
①苯②硝基苯③溴苯④溴乙烷⑤正己烷⑥四氯化碳⑦CH3Cl⑧丁烯⑨甲苯
A.②③④⑥; B.②③④⑥⑨; C.①②③④⑤⑥⑨; D.②③⑥⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
要检验溴乙烷中的溴元素,正确的实验方法是
A.加入氯水振荡,观察水层是否有棕红色出现
B.滴入硝酸银溶液,再加入稀硝酸呈酸性,观察有无浅黄色沉淀生成
C.加入氢氧化钠溶液共热,然后,加入稀硝酸呈酸性,再滴入硝酸银溶液,观察有无浅黄色沉淀生成
D.加入氢氧化钠溶液共热,冷却后滴入硝酸银溶液,观察有无浅黄色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
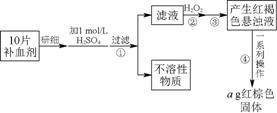
图95
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加____________,该过程的现象为________________________。
(2)步骤②加入过量H2O2的目的是________________________________________________________________________
________________________________________________________________________。
(3)步骤③中反应的离子方程式是________________________________________________________________________
________________________________________________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、________________________________________________________________________、
灼烧、________、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com