
分析 有机物A、B、C分子中碳、氢、氧原子数目之比为$\frac{40%}{12}$:$\frac{6.7%}{1}$:$\frac{53.3%}{16}$=1:2:1,故最简式为CH2O,由已知可得MA=22.4 L/mol╳1.34g/L=30g/mol,所以 A的分子式为CH2O,又A能发生银镜反应,应为醛类,即A为甲醛;又MB=MC=2MA 则B、C的分子式为C2H4O2,B显酸性,C显中性,则B为乙酸,C为甲酸甲酯.
解答 解:(1)有机物A、B、C分子中碳、氢、氧原子数目之比为$\frac{40%}{12}$:$\frac{6.7%}{1}$:$\frac{53.3%}{16}$=1:2:1,故最简式为CH2O,由已知可得MA=22.4 L/mol╳1.34g/L=30g/mol,所以 A的分子式为CH2O,在同温同压下,B、C的蒸气密度都是A的2倍,则B、C的分子式为C2H4O2,
答:A、B、C的分子式分别为:CH2O、C2H4O2、C2H4O2;
(2)A能发生银镜反应,应为醛类,即A为甲醛,结构简式为HCHO;
B、C的分子式为 C2H4O2,B显酸性,C显中性,C能与NaOH溶液反应生成醇和盐,则B为乙酸,C为甲酸甲酯,故B的结构简式为CH3COOH,C的结构简式为HCOOCH3,
答:A为HCHO,B为CH3COOH,C为HCOOCH3.
点评 本题考查有机物推断,为高频考点,侧重于学生的分析、计算能力的考查,计算确定有机物的分子式,再结合有机物性质推断,侧重对基础知识的巩固.


科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①③④ | C. | ①④⑥ | D. | ④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、MnO4-、SO42- | B. | NH4+、Al3+、NO3-、Cl- | ||
| C. | K+、Na+、AlO2-、NO3- | D. | Mg2+、K+、HCO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
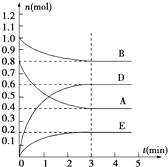 在容积为2L的密闭容器内,T℃时发生反应:mA(g)+nB(g)?pD(g)+qE(s)△H<0(m、n、p、q为最简比例的整数)反应过程如图所示:
在容积为2L的密闭容器内,T℃时发生反应:mA(g)+nB(g)?pD(g)+qE(s)△H<0(m、n、p、q为最简比例的整数)反应过程如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应正好达平衡 | |
| B. | 反应向左进行 | |
| C. | 反应向某方向进行一段时间后K<57.0 | |
| D. | 反应向某方向进行一段时间后c(H2)<0.2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 有两种同分异构体 | B. | 是非极性分子 | ||
| C. | 只有一种结构,无同分异构体 | D. | 是一种制冷剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
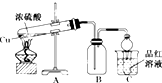 某化学兴趣小组为探索铜与浓硫酸的反应,用如图所示装置进行有关实验.
某化学兴趣小组为探索铜与浓硫酸的反应,用如图所示装置进行有关实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com