
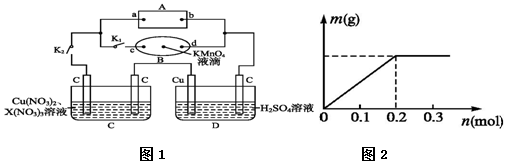
���� ��1���ر�K1����K2��Ϊ��ⱥ��ʳ��ˮװ�ã�ͨ���B��KMnO4�Ϻ�ɫҺ����c���ƶ������ݵ��ع���ԭ����֪�������������ƶ��жϵ�Դ������������дd�˵ĵ缫��Ӧʽ��
��2����K1���ر�K2����Ϊ���C��D���أ����ݵ��C��ͼ���֪����ʼ���������壬�ܹ�0.2mol����ͨ��ʱ�������������������֤����ʱ�����Ĺ�����ͭ���˺����е���ͨ���������й���������˵��X3+���ŵ磬H+�ŵ磬�Ӷ��ж����������ԣ�
��3��Dװ������Һ��H2SO4���缫C����b����������Ϊ��������ʼ�����ӵõ���������������������ͭʧ��������ͭ���ӽ��������������������ݴ˷�����
��� �⣺��1��������B��KMnO4�Ϻ�ɫҺ����c���ƶ���˵���������������c���ƶ������Ƴ���c��Ϊ����������֮�����ĵ�Դa��Ϊ������b��Ϊ����������ͨ����ֽd��Ϊ�������缫��ӦʽΪ2H++2e-=H2�����ʴ�Ϊ������2H++2e-=H2����
��2�����ݵ��C��ͼ���֪��ͨ�����й������ɣ���ͨ������Ϊ0.2molʱ�������������������֤����ʱ�����Ĺ�����ͭ�������X3+������������Ӧ����0.3mol������������ΪCu2+��X3+�������ӳ���0.2molʱ����������û�䣬˵�����������������������������ˮ��˵����������H+��X3+������������ΪCu2+��H+��X3+���ʴ�Ϊ��Cu2+��H+��X3+��
��3��Dװ������Һ��H2SO4���缫C����b����������Ϊ��������ʼΪ�����ӵõ���������������������ͭʧ��������ͭ���ӽ����������������������Կ���������Ϊ��C�˿�ʼʱ����ɫ��ζ���������һ��ʱ����к�ɫ�����������ʴ�Ϊ����C�˿�ʼʱ����ɫ��ζ���������һ��ʱ����к�ɫ����������
���� �����ۺϿ�����ԭ���Լ�����ͼ���ȡ��Ϣ������֪ʶ�ۺϷ�������������KMnO4�Ϻ�ɫҺ����c���ƶ��жϵ�Դ��������Ϊ������Ĺؼ���ע��缫����ʽ���жϣ�Ϊ�״��㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڲⶨ�к���ʵ������Ҫʹ�õ������У���ƽ����Ͳ���ձ����ζ��ܡ��¶ȼ� | |
| B�� | Ϊ��ȷ�ⶨ��Ӧ�����Һ���¶ȣ�ʵ�����¶ȼ�ˮ����Ӧ��С�ձ��ײ��Ӵ� | |
| C�� | ��50 mL 0.55 mol•L-1��NaOH��Һ��60 mL 0.50 mol•L-1�����ᷴӦ����õ��к�����ֵƫ�� | |
| D�� | ʹ�û��β����������Ϊ�˼Ӵ�Ӧ���ʣ���Сʵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4��g��+$\frac{3}{2}$O2��g���T2H2O��l��+CO��g����H1 | B�� | 2CO��g��+O2��g���T2CO2��g����H2 | ||
| C�� | S��s��+$\frac{3}{2}$O2��g���TSO3��s����H3 | D�� | C6H12O6��s��+6O2��g���T6CO2��g��+6H2O��l����H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2 | B�� | HCl | C�� | O2 | D�� | CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| X | ij����֮һ�ǿ�������Ҫ�ɷ֣��������ȼ�� |
| Y | ��ij�ֺ��ز������� |
| Z | ʧȥһ�����Ӻ��γ�Neԭ�ӵ��Ӳ�ṹ |
| W | �����������Ǵ�����������2�� |
 ��
��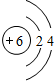 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
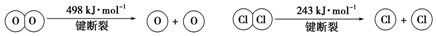
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com