
【题目】通过以下反应可获得新型能源二甲醚(![]() )。下列说法不正确的是
)。下列说法不正确的是
①![]()
![]()
②![]()
![]()
③![]()
![]()
④![]()
![]()
A. 反应①、②为反应③提供原料气
B. 反应③也是![]() 资源化利用的方法之一
资源化利用的方法之一
C. 反应![]() 的
的![]()
D. 反应![]() 的
的![]()
【答案】C
【解析】
A.反应③中的反应物为CO2、H2;
B.反应③中的反应物为CO2,转化为甲醇;
C.由反应④可以知道,物质的量与热量成正比,且气态水的能量比液态水的能量高;
D.由盖斯定律可以知道,②×2+③×2+④得到![]() 。
。
A.反应③中的反应物为CO2、H2,由反应可以知道,反应①、②为反应③提供原料气,所以A选项是正确的;
B.反应③中的反应物为CO2,转化为甲醇,则反应③也是CO2资源化利用的方法之一,所以B选项是正确的;
C. 由反应④可以知道,物质的量与热量成正比,且气态水的能量比液态水的能量高,则反应反应![]() 的
的![]() ,故C错误;
,故C错误;
D. 由盖斯定律可以知道,②×2+③×2+④得到![]() ,则
,则![]() ,所以D选项是正确的。
,所以D选项是正确的。
所以答案选C。


科目:高中化学 来源: 题型:
【题目】某元素的一种同位素X原子的质量数为A,它与2H原子组成2HmX分子,此分子含N个中子,在a g 2HmX中所含电子的物质的量是
A. ![]() (A-N+m) molB.
(A-N+m) molB. ![]() (A-N) mol
(A-N) mol
C. ![]() (A-N+m) molD.
(A-N+m) molD. ![]() (A-N+2m) mol
(A-N+2m) mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯胺![]() 是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
已知:①![]() 和NH3相似,与盐酸反应生成易溶于水的盐
和NH3相似,与盐酸反应生成易溶于水的盐![]()
②用硝基苯制取苯胺的反应原理: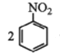 +3Sn+12HCl
+3Sn+12HCl![]()
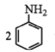 +3SnCl4+4H2O
+3SnCl4+4H2O
③有关物质的部分物理性质见下表:
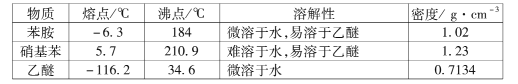
I.比较苯胺与氨气的性质
(1)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近,产生白烟,反应的化学方程式为____;用苯胺代替浓氨水重复上述实验,却观察不到白烟,原因是____。
Ⅱ.制备苯胺
往图1所示装置(夹持装置略,下同)的冷凝管口分批加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,往三颈烧瓶中滴入一定量50% NaOH溶液,至溶液呈碱性。
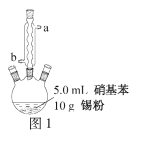
(2)冷凝管的进水口是____(填“a”或“b”);
(3)滴加NaOH溶液的主要目的是析出苯胺,反应的离子方程式为____。
Ⅲ.提取苯胺
i.取出图1所示装置中的三颈烧瓶,改装为图2所示装置。加热装置A产生水蒸气,烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液。
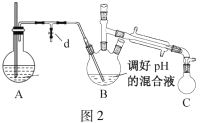
ii.往所得水溶液中加入氯化钠固体,使溶液达到饱和状态,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺2.79g。
(4)装置B无需用到温度计,理由是____。
(5)操作i中,为了分离混合物,取出烧瓶C前,应先打开止水夹d,再停止加热,理由是____。
(6)该实验中苯胺的产率为____。
(7)欲在不加热条件下除去苯胺中的少量硝基苯杂质,简述实验方案:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜和镁的合金4.6 g完全溶于浓硝酸,若反应中硝酸被还原只产生4 480 mL NO2气体和336 mL的N2O4气体(气体的体积已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为 ( )
A.9.02 gB.8.51 gC.8.26 gD.7.04 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由粗硅制备硅烷(SiH4)的基本流程如图所示:

已知:反应Ⅰ的化学方程式为Si+3HCl= SiHCl3+X,反应Ⅱ的化学方程式为SiHCl3+Y = Si+3HCl(均已配平)。下列说法不正确的是
A.X和Y为同一种物质
B.SiH4的稳定性比NH3强
C.流程中的4个反应有3个属于氧化还原反应
D.反应Ⅳ中SiH4、NH3两种气体在常温常压下体积比为1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是

A.31d和33d属于同种核素
B.气态氢化物的稳定性:a>d>e
C.工业上常用电解法制备单质b
D.a和b形成的化合物不可能含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)下列反应属于放热反应的是_______。
A.铝片与稀H2SO4反应制取H2B.碳酸钙高温分解成氧化钙和二氧化碳 C.葡萄糖在人体内氧化分解D.Ba(OH)2·8H2O与NH4Cl固体反应
(2)一定条件下,2L密闭容器中SO2与O2反应5min后,若SO2和SO3物质的量分别为0.1 mol和0.3mol,则SO2起始物质的量浓度为___;用O2表示这段时间该化学反应速率为______。
(3)用活性炭还原法处理氮氧化物。有关反应为C(s)+2NO(g)![]() N2(g)+CO2(g),某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,下列说法不能作为判断该反应达到化学平衡状态标志的是________(填选项字母)
N2(g)+CO2(g),某研究小组向恒容密闭容器中加入一定量的活性炭和NO,恒温(T℃)条件下反应,下列说法不能作为判断该反应达到化学平衡状态标志的是________(填选项字母)
A.活性炭的质量保持不变 B.v正(N2)=2v逆(NO) C.容器内气体压强保持不变 D.容器内混合气体的密度保持不变 E.容器内混合气体的平均相对分子质量保持不变 F.容器内CO2的浓度保持不变
(4)利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能利用化学能,装置如图所示:

①A电极的电极反应式为_______________。
②下列关于该电池的说法正确的是___________(填选项字母)。
A.电子从右侧电极经过负载后流向左侧电极 B.离子交换膜为阴离子交换膜,则OH-由右侧溶液移向左侧溶液 C. 当有4.48L NO2被处理时,转移电子的物质的量为0.8mol
(5)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。已知: 1molN2和3molH2反应生成2molNH3时放出热量93kJ,试根据表中所列键能数据计算a的数值_______。
化学键 | H—H | N—H | N≡N |
键能kJ/mol | 436 | a | 945 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) ![]() 2C(g)+2D(g)ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g)ΔH=Q,2 min末达到平衡,生成0.8 mol D。
(1)300 ℃时,该反应的平衡常数表达式为:K=______。已知K300 ℃<K350 ℃,则ΔH______0(填“>”或“<”)。
(2)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”),原因是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贝壳、珍珠、方解石等主要成分均含有CaCO3,回答下列问题:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧碳酸钙时的焰色为_______(填标号)。
A 黄色 B 红色 C 紫色 D 绿色
(2)CaCO3中三种元素第一电离能由小到大的顺序是__________。CaCO3中的化学键除了σ键外,还存在_________________。
(3)关于CO2和CO32-的下列说法正确的是__________。
a 两种微粒价层电子对数相同 b 两种微粒的中心原子均无孤电子对
c 键角:CO2>CO32- d 两种微粒的中心原子杂化方式相同
(4)难溶碳酸盐易分解,CaCO3、BaCO3热分解温度更高的是_____,原因是______。
(5)方解石的菱面体结构如图1,沿三次轴的俯视图为正六边形。方解石的六方晶胞结构如图2,晶胞底面为平行四边形,其较小夹角为60°,边长为anm,晶胞高为c nm。
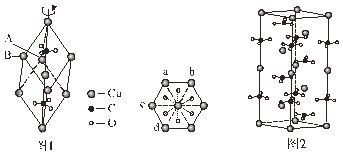
A点在俯视图中为a,则B点在俯视图中的位置为_________(填字母)。方解石的六方晶胞中,Ca2+和CO32-个数比为___________;若阿伏加德罗常数为NA,则该方解石的密度为________g/cm3(列出计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com