
ЁОЬтФПЁПвбжЊГЃЮТГЃбЙЯТЃЌN2КЭH2ЩњГЩ2molNH3ЗХГі92.4KJШШСПЃЌдкЭЌЮТЯТЯђКуШнУмБеШнЦїжаЭЈШы1molN2КЭ3molH2ЃЌДяЦНКтЪБЗХГіШШСПЮЊQ1KJЃЌЯђСэвЛЬхЛ§ЯрЭЌЕФШнЦїжаЭЈШы0.5molN2ЁЂ1.5molH2КЭ1molNH3,ЯрЭЌЬѕМўЯТ,ДяЦНКтЪБЗХГіШШСПЮЊQ2KJЃЌдђЯТСае§ШЗЕФЪЧ
A. 2Q2ЉQ1Љ92.4 B. 2Q2=Q1=92.4 C. Q1ЉQ2Љ92.4 D. Q1=Q2Љ92.4
ЁОД№АИЁПA
ЁОНтЮіЁП
ЯђУмБеШнЦїМзжаЭЈШы1mol N2КЭ3mol H2ЃЌДяЕНЦНКтЪБЃЌЧтЦјКЭЕЊЦјВЛФмЭъШЋзЊЛЏЃЛДяЕНЦНКтЪБЗХГіШШСПQ1kJаЁгк92.4kJЃЛМйЖЈ0.5mol N2КЭ1.5mol H2ЭъШЋЗДгІЃЌДяЕНЦНКтЪБЗХГіШШСПQ2 kJЃЌИљОнN2ЃЈgЃЉ+3H2ЃЈgЃЉ2NH3ЃЈgЃЉЁїH=-92.4kJmol-1ПЩжЊЃЌЗХГіЕФШШСПЮЊЃК![]() =46.2kJЃЌгЩгкКЯГЩАБЪЧПЩФцЗДгІЃЌЙЪЗДгІЮяВЛФмЭъШЋЗДгІЃЌЫљвдЗХГіЕФШШСПQ2аЁгк46.2kJЃЛЕУЕНQ1ЃО2Q2ЃЛзлЩЯЫљЪіПЩжЊЃК2Q2ЉQ1Љ92.4ЃЛД№АИбЁAЁЃ
=46.2kJЃЌгЩгкКЯГЩАБЪЧПЩФцЗДгІЃЌЙЪЗДгІЮяВЛФмЭъШЋЗДгІЃЌЫљвдЗХГіЕФШШСПQ2аЁгк46.2kJЃЛЕУЕНQ1ЃО2Q2ЃЛзлЩЯЫљЪіПЩжЊЃК2Q2ЉQ1Љ92.4ЃЛД№АИбЁAЁЃ


 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаа№Ъіе§ШЗЕФЪЧ
A.ЯЁСђЫсШмвКжаВЛДцдкH2SO4Зжзг
B.ЗВЪЧФмЕчРыЕФЮяжЪвЛЖЈФмДяЕНЕчРыЦНКт
C.ТШЛЏФЦШмвКдкЕчСїзїгУЯТЕчРыГЩФЦРызгКЭТШРызг
D.АБЫЎжаШЋВПЪЧNH4+ЁЂOH-ЃЌЮоЗжзгДцдк
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏЪЏШМСЯжЎвЛЕФЬьШЛЦјЃЌЦфжївЊГЩЗжЪЧМзЭщЃЎЧыЛиД№ЯТСаЮЪЬтЃЎ
(1)МзЭщЕФЕчзгЪНЪЧЃК______________________ЃЎ
(2)МзЭщгыТШЦјдкЙтееЯТЗДгІЕФВњЮяга_______________жжЃЌИУЗДгІЕФРраЭЪЧ________ЃЎ
(3)МзЭщЕФПеМфЙЙаЭЪЧ________________ЃЌПЩжЄУїЦфЙЙаЭЕФЪЕбщЪТЪЕЪЧЃК___________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЗДгІЪєгкбѕЛЏЛЙдЗДгІЕФЪЧЃЈ ЃЉ
A.CaCO3 ![]() CaO+CO2ЁќB.SO3 + H2O=H2SO4
CaO+CO2ЁќB.SO3 + H2O=H2SO4
C.AgNO3+NaCl=AgClЁ§+NaNO3D.Fe+CuSO4=FeSO4+Cu
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИљОнЕтгыЧтЦјЗДгІЕФШШЛЏбЇЗНГЬЪНЃЌЯТСаХаЖЯе§ШЗЕФЪЧ
ЂйI2(g)+ H2(g) ![]() 2HI(g) ЁїH = Ѓ9.48 kJ/mol
2HI(g) ЁїH = Ѓ9.48 kJ/mol
ЂкI2(s)+ H2(g) ![]() 2HI(g) ЁїH = +26.48 kJ/mol
2HI(g) ЁїH = +26.48 kJ/mol
A. 254 g I2(g)жаЭЈШы2 g H2(g)ЃЌЗДгІЗХШШ9.48 kJ
B. 1 molЙЬЬЌЕтгы1 molЦјЬЌЕтЫљКЌЕФФмСПЯрВю17.00 kJ
C. ЗДгІЂйЕФВњЮяБШЗДгІЂкЕФВњЮяЮШЖЈ
D. ЗДгІЂкЕФЗДгІЮязмФмСПБШЗДгІЂйЕФЗДгІЮязмФмСПЕЭ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПXЁЂYЁЂZЁЂWЪЧдзгађЪ§вРДЮдіДѓЕФГЃМћЖЬжмЦкдЊЫиЃЌXЕФФГжжЧтЛЏЮяФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЃЎYЕФвЛжжКЫЫижЪСПЪ§ЮЊ18ЃЌжазгЪ§ЮЊ10ЃЎдкЭЌжмЦкдЊЫижаZЕФМђЕЅРызгАыОЖзюаЁЃЌWЕФЕЅжЪЪЧСМКУЕФАыЕМЬхВФСЯЁЃЯТСаЫЕЗЈжае§ШЗЕФЪЧ
A. МђЕЅЦјЬЌЧтЛЏЮяЮШЖЈадЃКW >X
B. YдЊЫиЕФЯрЖддзгжЪСПЮЊ18
C. X2H4ЕФЗжзгжаМЋадМќКЭЗЧМЋадМќЪ§ФПБШЮЊ4ЃКl
D. ЕчНтZЕФШлШкТШЛЏЮяПЩвдвБСЖЕЅжЪZ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкШнЛ§вЛЖЈЕФУмБеШнЦїжаЗЂЩњПЩФцЗДгІЃКA(g)ЃЋ2B(g) ![]() 2C(g)ЁЁІЄH>0ЃЌЦНКтвЦЖЏЙиЯЕШчЭМЫљЪОЁЃдђЯТСаЫЕЗЈе§ШЗЕФЪЧ
2C(g)ЁЁІЄH>0ЃЌЦНКтвЦЖЏЙиЯЕШчЭМЫљЪОЁЃдђЯТСаЫЕЗЈе§ШЗЕФЪЧ

A. p1>p2ЃЌзнзјБъПЩБэЪОAЕФжЪСПЗжЪ§
B. p1<p2ЃЌзнзјБъПЩБэЪОCЕФжЪСПЗжЪ§
C. p1>p2ЃЌзнзјБъПЩБэЪОЛьКЯЦјЬхЕФЦНОљФІЖћжЪСП
D. p1<p2ЃЌзнзјБъПЩБэЪОAЕФзЊЛЏТЪ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉдк25ЁцЁЂ101kPaЯТЃЌ16gЕФМзДМЃЈCH3OHЃЉЭъШЋШМЩеЩњГЩCO2КЭвКЬЌЫЎЪБЗХГі352kJЕФШШСПЃЌдђБэЪОМзДМШМЩеШШЕФШШЛЏбЇЗНГЬЪНЮЊ_______________________________ЃЎ
ЃЈ2ЃЉвбжЊЃКЂйCH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ЁїH1=-870.3kJ/molЃЛ
ЂкC(s)+O2(g)=CO2(g) ЁїH2=-393.5kJ/mol
ЂлH2(g)+1/2O2(g)=H2O(l) ЁїH3=-285.8kJ/molЃЌ
дђ2C(s)+2H2(g)+O2(g)= CH3COOH(l)ЕФЗДгІШШЪЧ______________
ЃЈ3ЃЉШчЭМЪЧN2КЭH2ЗДгІЩњГЩ2mol NH3Й§ГЬжаФмСПБфЛЏЪОвтЭМЃЌ
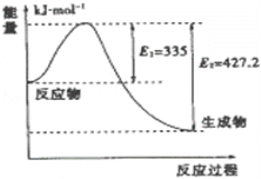
ЂйЧыМЦЫуУПЩњГЩ1mol NH3ЗХГіШШСПЮЊЃК________ЃЌФцЗДгІЫљашЕФЛюЛЏФмЮЊ__________________ kJ/molЁЃ
ЂкШєЦ№ЪМЪБЯђШнЦїФкЗХШы1mol N2КЭ3mol H2ЃЌДяЦНКтКѓN2ЕФзЊЛЏТЪЮЊ20%ЃЌдђЗДгІЗХГіЕФШШСПЮЊQ1 kJЃЌдђQ1ЕФЪ§жЕЮЊ__________________ЃЛ
ЃЈ4ЃЉгУ50mL0.50mol/LбЮЫсгы50mL0.55mol/LNaOHШмвКНјаажаКЭЗДгІЁЃЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЫљЗХГіЕФШШСППЩМЦЫужаКЭШШЁЃЛиД№ЯТСаЮЪЬтЃК
ЂйШчгУДзЫсДњЬцбЮЫсНјааЪЕбщЃЌЫљВтжаКЭШШЕФЪ§жЕНЋ________(ЬюЁАЦЋДѓЁБЁАЦЋаЁЁБЛђЁАЮогАЯьЁБЃЌЯТЭЌ)ЃЛ
ЂкШчгУ70mL0.50mol/LбЮЫсНјааЪЕбщЃЌЫљВтжаКЭШШЪ§жЕНЋ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯжгаЗДгІЃКmA (g) +nB (g)![]() pc (g) ЃЌДяЕНЦНКтКѓЃЌЕБЩ§ИпиЖШЪБЃЌBЕФзЊЛЏТЪБфДѓЃЛЕБМѕаЁбЙЧПЪБЃЌЛьКЯЬхЯЕжаCЕФжЪСПЗжЪ§вВМѕаЁЃЌдђЃК
pc (g) ЃЌДяЕНЦНКтКѓЃЌЕБЩ§ИпиЖШЪБЃЌBЕФзЊЛЏТЪБфДѓЃЛЕБМѕаЁбЙЧПЪБЃЌЛьКЯЬхЯЕжаCЕФжЪСПЗжЪ§вВМѕаЁЃЌдђЃК
ЃЈ1ЃЉИУЗДгІЕФФцЗДгІЮЊ____ШШЗДгІЃЌЧвm+n____p (ЬюЁА>ЁБЁЂ ЁА=ЁБ ЁЂЁА<ЁБЃЉЁЃ
ЃЈ2ЃЉМѕбЙЪБЃЌAЕФжЪСПЗжЪ§______.(ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБЃЌЯТЭЌЃЉ
ЃЈ3ЃЉШєМгШыB (ЬхЛ§ВЛБфЃЉЃЌдђAЕФзЊЛЏТЪ_____ЃЌBЕФзЊЛЏТЪ_________ЁЃ
ЃЈ4ЃЉШєЩ§ИпиЖШЃЌдђЦНКтЪБBЁЂCЕФХЈЖШжЎБШНЋ__________ЁЃ
ЃЈ5ЃЉШєМгШыДпЛЏМСЃЌЦНКтЪБЦјЬхЛьКЯЮяЕФзмЮяжЪЕФСП______________ЁЃ
ЃЈ6ЃЉШєBЪЧгаЩЋЮяжЪЃЌAЁЂCОљЮоЩЋЃЌдђМгШыC (ЬхЛ§ВЛБфЃЉЪБЛьКЯЮябеЩЋ______ЃЌЖјЮЌГжШнЦїФкбЙЧПВЛБфЃЌГфШыФЪЦјЪБЃЌЛьКЯЮябеЩЋ______(ЬюЁАБфЩюЁБЁЂ ЁАБфЧГЁБЛђЁАВЛБфЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com