
【题目】物质分类是化学研究的重要方法之一。化学工作者经常根据物质的组成对物质进行分类研究。近年来发现,在金星大气层中存在三氧化二碳。下列物质与它属于同类的是( )
A.H2、O3
B.H2SO4、H2CO3
C.SO2、NO
D.Na2SO3、KClO3
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3,请回答下列问题:
①较Na3N中两种微粒的半径r(Na+) r(N3-) (填“>”“<”或“=”),
②a3N与水反应属于 反应(填“氧化还原”或“非氧化还原”);
③酸反应生成两种盐的化学式为 ;
④写出化合物Na3N的电子式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以 H2、O2、熔融盐 Na2CO3 组成燃料电池,采用电解法制备 Fe(OH)2,装置如下图所示,其中 P端通入CO2。通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是

A.X、Y 两端都必须用铁作电极
B.不可以用 NaOH 溶液作为电解液
C.阴极发生的反应是:2H2O+2e-=H2↑+ 2OH-
D.X 端为电解池的阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
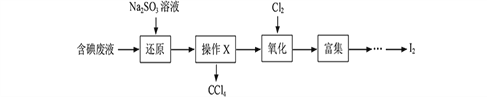
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为________________;该操作将I2还原为I-的目的是_____________________。
(2)操作X的名称为____________。
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在400C左右反应(实验装置如下图所示)。实验控制在较低温度下进行的原因是________________;锥形瓶里盛放的溶液为______________。

(4)已知:5SO32—+2IO3—+2H+![]() I2+5SO42—+H2O
I2+5SO42—+H2O
某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3—中的一种或两种。请补充完整检验含碘废水中是否含有IO3—的实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在;_____________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属和硝酸反应,已知被还原的硝酸和参加反应的硝酸的物质的量之比为1∶6,若己知还原产物唯一,则还原产物为
A. N2 B. N2O C. NO D. NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方法不正确的是
A. 除去NH4Cl溶液中的FeCl3,可向溶液中加入氨水调节pH
B. 除去金属离子Cu2+、Hg2+,可向溶液中加入Na2S、H2S等沉淀剂
C. 除去某溶液中的SO42-可向溶液中加入镁盐
D. 除去ZnCl2溶液中的Fe3+可向溶液中加入Zn(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 在一定温度条件下,对于已达平衡的反应:FeCl3+3KSCN![]() 3KCl+Fe(SCN)3,在此溶液中作如下处理,平衡左移的是( )
3KCl+Fe(SCN)3,在此溶液中作如下处理,平衡左移的是( )
A.加入少量氯化钾固体 B.加入少量氯化铁固体
C.只减少Fe(SCN)3的浓度 D.加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化镁溶液的密度为1.1 g·mL-1,其中镁离子的质量分数为4.8%,100 mL该溶液中Cl-的物质的量约为( )
A. 0.37 mol B. 0.63 mol
C. 0.74 mol D. 0.44mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com