
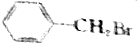 ¢ŚCH3CH2CH3Br ¢ŪCH3Br ¢ÜCH3CHBrCH2CH3
¢ŚCH3CH2CH3Br ¢ŪCH3Br ¢ÜCH3CHBrCH2CH3·ÖĪö £Ø1£©¾łĪŖĀ±“śĢž£¬CŌ×ÓøöŹżŌ½¶ą£¬·ŠµćŌ½“ó£¬ĆܶČŌ½“ó£»
£Ø2£©Óė-BrĻąĮ¬CµÄĮŚĪ»CÉĻÓŠHæÉ·¢ÉśĻūČ„·“Ó¦£¬Ā±“śĢžæÉ·¢ÉśĖ®½ā·“Ó¦£»
£Ø3£©Ā±“śĢžŌŚNaOH/“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ó¦£¬½įŗĻ½į¹¹·ÖĪö²śĪļ£»
£Ø4£©CH3CH2CH3BrÖʱø±ū¶ž“¼£¬ĻČ·¢ÉśĻūČ„·“Ӧɜ³ÉĻ©Ģž”¢ŌŁ¼Ó³É”¢Ė®½ā£»
£Ø5£©¼ģŃéĪļÖŹ¢ŪÖŠŗ¬ÓŠäåŌŖĖŲ£¬æÉĖ®½āŗó¼ģŃéäåĄė×Ó£®
½ā“š ½ā£ŗ£Ø1£©¾łĪŖĀ±“śĢž£¬CŌ×ÓøöŹżŌ½¶ą£¬·ŠµćŌ½“ó£¬ĆܶČŌ½“ó£¬ŌņĪļÖŹµÄČŪ”¢·ŠµćÓÉøßµ½µĶµÄĖ³ŠņŹĒ¢Ł¢Ü¢Ś¢Ū£¬ĆܶČÓɓ󵽊”µÄŹĒ¢Ł¢Ü¢Ś¢Ū£¬
¹Ź“š°øĪŖ£ŗ¢Ł¢Ü¢Ś¢Ū£»¢Ł¢Ü¢Ś¢Ū£»
£Ø2£©Óė-BrĻąĮ¬CµÄĮŚĪ»CÉĻÓŠHæÉ·¢ÉśĻūČ„·“Ó¦£¬Ā±“śĢžæÉ·¢ÉśĖ®½ā·“Ó¦£¬ŌņÖ»ÓŠ¢Ś¢ÜæÉ·¢ÉśĻūČ„”¢Č”“ś·“Ó¦£¬¹Ź“š°øĪŖ£ŗ¢Ś¢Ü£»
£Ø3£©ĪļÖŹ¢ÜŌŚNaOH/“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ó¦£¬²śĪļĪŖCH2=CHCH2CH3»ņCH3CH=CHCH3£¬¹Ź“š°øĪŖ£ŗNaOH/“¼ČÜŅŗ£»CH2=CHCH2CH3»ņCH3CH=CHCH3£»
£Ø4£©CH3CH2CH3BrÖʱø±ū¶ž“¼£¬ĻČ·¢ÉśĻūČ„·“Ӧɜ³ÉCH2=CHCH3”¢ŌŁ·¢Éś¼Ó³É·“Ӧɜ³ÉClCH2CHClCH3£¬×īŗó·¢ÉśĖ®½ā·“Ӧɜ³ÉHOCH2CHOHCH3£¬
¹Ź“š°øĪŖ£ŗĻūČ„·“Ó¦”¢¼Ó³É·“Ó¦”¢Ė®½ā·“Ó¦£»
£Ø5£©¼ģŃéĪļÖŹ¢ŪÖŠŗ¬ÓŠäåŌŖĖŲ£¬æÉĖ®½āŗó¼ģŃéäåĄė×Ó£¬ŌņŠčŅŖŹŌ¼ĮĪŖNaOHČÜŅŗ”¢ĻõĖį”¢ĻõĖįŅų£¬ŌŚNaOHČÜŅŗÖŠĖ®½āŗó¼ÓĻõĖįÖĮĖįŠŌ£¬ŌŁ¼ÓĻõĖįŅų¹Ū²ģŹĒ·ń²śÉśµ»ĘÉ«³Įµķ£¬¹Ź“š°øĪŖ£ŗNaOHČÜŅŗ”¢ĻõĖį”¢ĻõĖįŅų£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄ½į¹¹ÓėŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ¹ŁÄÜĶÅÓėŠŌÖŹµÄ¹ŲĻµ”¢ÓŠ»ś·“Ó¦”¢Ąė×ӵļģŃé¼°ĪļĄķŠŌÖŹ±Č½Ļ·½·ØĪŖ½ā“š±¾Ģā¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®


 ŗĆ³É¼Ø1¼Ó1ĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
ŗĆ³É¼Ø1¼Ó1ĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø ½š×“ŌŖ¼ØÓÅŗĆ¾ķĻµĮŠ“š°ø
½š×“ŌŖ¼ØÓÅŗĆ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1LÖŠŗ¬ÓŠ4 g NaOHµÄČÜŅŗ | |
| B£® | Ļ”ŹĶ1mL£¬1mol/L NaOHČÜŅŗµ½1LŗóĖłµĆČÜŅŗ | |
| C£® | pH=11µÄČÜŅŗ | |
| D£® | 0.11 mol/LNaOHČÜŅŗøśµČĢå»ż0.05mol/L H2SO4ČÜŅŗµÄ»ģŗĻŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | A | B | C | D |
| ÄæµÄ | ŹµŃéŹŅÖĘO2 | ÅäÖĆĻ”ĮņĖįČÜŅŗ | ŌŚĢśÖĘĘ·ÉĻ¶ĘĶ | ¼ģ²é×°ÖĆĘųĆÜŠŌ |
| ×°ÖĆ»ņ²Ł×÷ | 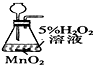 | 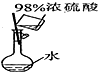 | 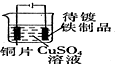 | 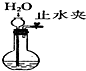 |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 10gH2ŗĶ10gO2 | B£® | 5.6LN2£Ø±ź×¼×“æö£©ŗĶ11gCO2 | ||
| C£® | 9gH2OŗĶ0.5molBr2 | D£® | 22.4mLH2£Ø±ź×¼×“æö£©ŗĶ0.1molN2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe£ØOH£©3 | B£® | Fe£ØOH£©2 | C£® | FeCl2 | D£® | FeCl3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
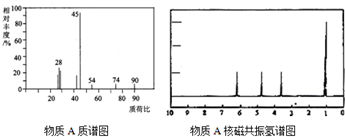
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
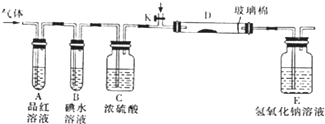
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com