���
�⣺��1��a�����᳣�����¶ȣ����ֽ⣬��a����
b����Ӧ�ж���������ֻ�ԭ�ԣ���ԭ�Ա�HIǿ���ⵥ�������Դ��ڶ�������b����
c��1molSO
2����2molH
2O����1molH
2SO
4��1molH
2SO
4�ֽ�����1molSO
2��1molH
2O��ѭ����ˮ�������٣���Ӧ����ˮ����c��ȷ��
d���ɢ��֪����lmolO
2��ͬʱ����2molSO
2����I��֪2molSO
2����4molHI���ɢ��֪4molHI�ֽ�����2mol H
2����ѭ�������в���l mol O
2��ͬʱ����2mol H
2����d����
�ʴ�Ϊ��c��
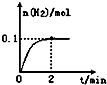
��2����ͼ��֪2min�����������ʵ���������0.1mol����������Ũ��Ϊ
=0.1mol/L����������ʾ�Ļ�ѧ��Ӧ����Ϊ
=0.05mol/��L��min����
�ɷ�Ӧ�еĻ�ѧ��������֪v��HI��=0.05mol/��L��min����2=0.1mol/��L��min�������ݷ���ʽ����ƽ��Ũ�ȣ�c��H
2��=0.1mol/L��c��I
2��=0.1mol/L��c��HI��=0.8mol/L��д��ƽ�ⳣ������ʽ���㣺K=
=
=
������¶��£�H
2��g��+I
2��g��?2HI��g����ƽ�ⳣ��K=64��
�Ը÷�Ӧ�����¶Ȳ��俪ʼ����HI��g�������ʵ�����ԭ����2�������¶Ȳ��䣬K���䣬��a�������ʵ���Ϊԭ����2�����÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ��
��Ӧ��ϵ�и����ʵ�Ũ�ȶ���ԭ����2������b��ȷ�����ʵ���������ѧ��Ӧ����������Ŀ죬����Ũ�ȵļ�С����������ij̶ȱ�С����c����
�ɷ�Ӧ����ʽ��ԭ��������������������ȣ�������������½�����ƽ��Ϊ��Чƽ�⣬��ƽ��ʱH
2�����������ͬ����d����
�ʴ�Ϊ��0.1mol?L
-1?min
-1��64��b��
��3��ʵ������Zn��ϡ������ȡH
2����Ӧ������������Ũ�ȼ�С����Ӧʱ��Һ��ˮ�ĵ���ƽ��������У�
���������������Լ�������������Ӧ����������
a������NaNO
3 ��Һ�൱��ϡ����ҺŨ�ȼ�С����Ӧ���ʼ�С����a�����ϣ�
b������CuSO
4 ��Һ����п��Ӧ����ͭ��ͭ��п��ϡ������Һ���γ�ԭ��ط�Ӧ������������������b���ϣ�
c������Na
2SO
4��Һ�൱��ϡ����ҺŨ�ȼ�С����Ӧ���ʼ�С����c�����ϣ�
d������NaHSO
3 ��Һ���������ᣬ���������ķ�Ӧ���ʼ�С����d�����ϣ�
�ʴ�Ϊ�����ң�b��

 ��--��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
��--��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��

 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д�
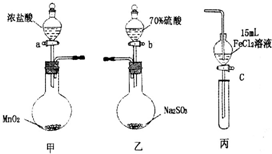 Ϊ��֤������C12��Fe3+��SO2ijС������ͼ��ʾװ�ý���ʵ�飨�г������ͼ��м���װ�����ԣ��������Ѽ��飩��
Ϊ��֤������C12��Fe3+��SO2ijС������ͼ��ʾװ�ý���ʵ�飨�г������ͼ��м���װ�����ԣ��������Ѽ��飩��